一种缺陷短波单胞菌冻存定量挑战原液的制备方法及其用途与流程
- 国知局
- 2024-10-21 15:04:39
本发明涉及液体细菌截留试验,尤其涉及一种缺陷短波单胞菌冻存定量挑战原液的制备方法及其用途。
背景技术:
1、液体细菌截留试验用于评价0.22μm除菌级过滤器的细菌截留能力。目前,标称孔径0.22μm药液过滤器在生产企业的出厂检验和产品注册检验时,液体细菌截留是必检的性能指标,该指标不合格将直接导致患者在输液过程中出现各种输液反应。
2、现生产企业和检测机构均采用yy/t 0918-2014《药液过滤膜、药液过滤器细菌截留试验方法》、yy/t 0929.3-2023《输液用药液过滤器第3部分:标称孔径0.22μm药液过滤器液体细菌截留试验方法》中的方法进行液体细菌截留试验。
3、在以上标准中均规定,用现配的缺陷短波单胞菌挑战原液进行液体细菌截留试验。以yy/t 0929.3-2023中的方法为例,具体步骤如下:
4、1)取缺陷短波单胞菌(atcc19146)保存菌种接种于营养琼脂培养基(na)或胰酪大豆胨琼脂培养基(tsa)平板上,30℃±2℃培养24h,得到缺陷短波单胞菌新鲜培养物。
5、2)从缺陷短波单胞菌新鲜培养物上挑取菌落,接种于10ml营养肉汤培养基(nb)或胰酪大豆胨液体培养基(tsb)中,30℃±2℃培养24h。
6、3)将10ml培养液移入1l tsb中混匀,30℃±2℃培养24h,即得到挑战原液。临用前可以在4℃保存,但不应超过8h。
7、4)从挑战原液中取样,用1g/l蛋白胨水进行梯度稀释,按《中华人民共和国药典》(2020年版)四部1105“非无菌产品微生物限度检查:微生物计数法"测定挑战原液的活菌浓度。培养基为na或tsa,培养条件为30℃±2℃,48h。
8、在实际操作过程中发现该方法有以下缺点:
9、(1)挑战原液活菌定量(第4步)共需培养2天时间,且标准中未明确测定挑战原液活菌浓度的48小时培养时间里,挑战原液的保存温度,仅规定了临用前可以在4℃保存,但不应超过8h。挑战原液在不适宜的保存温度下,活菌浓度值不稳定,可能增多也可能减少,直接影响试验结果;
10、(2)缺陷短波单胞菌定量挑战原液的制备共需培养5天,挑战原液的制备时间较长。
技术实现思路
1、为解决现有技术存在的标准中未规定挑战原液计数时的保存温度,活菌浓度在不适宜的温度下保存48小时后会活菌浓度会发生变化,直接影响试验结果,每次进行液体细菌截留试验,均需5天时间制备挑战原液,试验时间较长的技术问题,本发明提供了如下技术方案。
2、本发明一种缺陷短波单胞菌冻存定量挑战原液的制备方法,包括如下步骤:
3、s1:用胰酪大豆胨液体培养基培养标准菌株在3代以内的缺陷短波单胞菌,30℃±2℃下培养24小时后取出,制得缺陷短波单胞菌挑战原液,将缺陷短波单胞菌挑战原液进行离心浓缩,得到高浓度的缺陷短波单胞菌挑战原液;
4、s2:制备好高浓度的挑战原液后,分别量取浓度为99.9%的dmso溶液和浓度为99%的甘油溶液,混合均匀后得混合溶液,将混合溶液加入高浓度缺陷短波单胞菌挑战原液中,之后充分混匀;
5、s3:将混匀后的挑战原液分装、标识后放置于-70℃以下条件下保存。
6、作为进一步的技术方案,所述步骤s1中,所述高浓度的缺陷短波单胞菌挑战原液的活菌浓度是原有缺陷短波单胞菌挑战原液活菌浓度的两倍。
7、作为进一步的技术方案,所述步骤s2中,所述混合溶液与所述高浓度缺陷短波单胞菌挑战原液的体积比为1:1.
8、作为进一步的技术方案,所述步骤s2中,所述混合溶液中dmso溶液与甘油溶液的体积比为1~3:2~4。
9、作为进一步的技术方案,所述步骤s2中,所述混合溶液中dmso溶液与甘油溶液的体积比为2:3。
10、本发明还包括一种缺陷短波单胞菌冻存定量挑战原液的用途,所述缺陷短波单胞菌冻存定量挑战原液复溶后直接使用,用于液体细菌截留试验。
11、作为进一步的技术方案,所述缺陷短波单胞菌冻存定量挑战原液复溶后用于标称孔径0.22μm药液过滤器液体细菌截留试验。
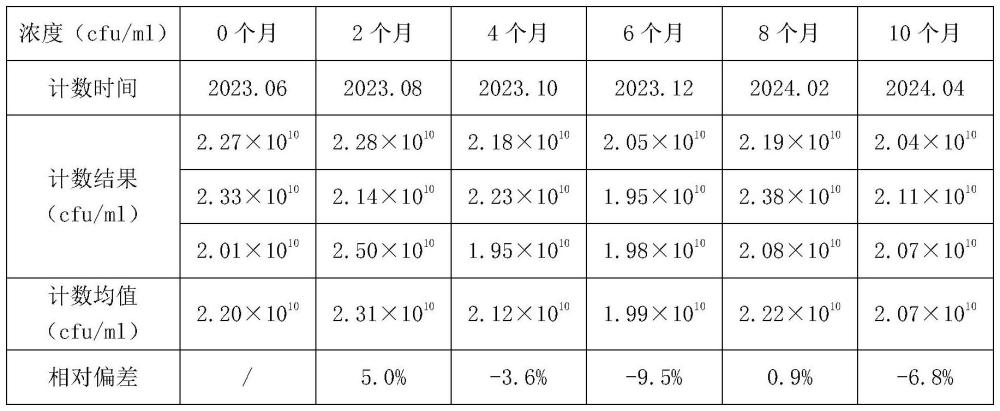
12、本发明的有益效果,本发明制备的缺陷短波单胞菌冻存定量挑战原液在-70℃以下条件下可长期保存,有效期10个月,且其浓度保持不变。每次试验可直接取用,操作简单,方便快捷,有效减少每次进行液体细菌截留试验时制备定量挑战原液用试剂耗材成本、试验员工作时间及挑战原液制备所需时间(5天)等,经研究发现,该冻存挑战原液的活菌浓度值稳定,可显著提高工作效率,同时大大提高试验结果的准确性,较大程度上节省试验人力、物力和时间成本,有较高的价值。
技术特征:1.一种缺陷短波单胞菌冻存定量挑战原液的制备方法,其特征在于,包括如下步骤:
2.根据权利要求1所述的缺陷短波单胞菌冻存定量挑战原液的制备方法,其特征在于:所述步骤s1中,所述高浓度的缺陷短波单胞菌挑战原液的活菌浓度是原有缺陷短波单胞菌挑战原液活菌浓度的两倍。
3.根据权利要求2所述的缺陷短波单胞菌冻存定量挑战原液的制备方法,其特征在于:所述步骤s2中,所述混合溶液与所述高浓度缺陷短波单胞菌挑战原液的体积比为1:1。
4.根据权利要求1所述的缺陷短波单胞菌冻存定量挑战原液的制备方法,其特征在于:所述步骤s2中,所述混合溶液中dmso溶液与甘油溶液的体积比为1~3:2~4。
5.根据权利要求4所述的缺陷短波单胞菌冻存定量挑战原液的制备方法,其特征在于:所述步骤s2中,所述混合溶液中dmso溶液与甘油溶液的体积比为2:3。
6.一种缺陷短波单胞菌冻存定量挑战原液的用途,其特征在于:所述缺陷短波单胞菌冻存定量挑战原液复溶后直接使用,用于液体细菌截留试验。
7.根据权利要求6所述的缺陷短波单胞菌冻存定量挑战原液的用途,其特征在于:所述缺陷短波单胞菌冻存定量挑战原液室温复融后作为挑战原液于标称孔径0.22μm药液过滤器液体细菌截留试验。
技术总结本发明公开了一种缺陷短波单胞菌冻存定量挑战原液的制备方法及其用途,其中制备方法包括如下步骤:S1:制备高浓度的缺陷短波单胞菌挑战原液;S2:分别量取浓度为99.9%的DMSO溶液和浓度为99%的甘油溶液,混合均匀后得混合溶液,将混合溶液加入高浓度缺陷短波单胞菌挑战原液中,之后充分混匀;S3:将混匀后的挑战原液分装、标识后放置于‑70℃以下条件下保存。本发明制备的缺陷短波单胞菌冻存定量挑战原液在‑70℃以下条件下可长期保存,有效期10个月,且其浓度保持不变,每次试验可直接取用,有效减少每次进行液体细菌截留试验时所需时间,可显著提高工作效率,同时大大提高试验结果的准确性,较大程度上节省试验人力、物力和时间成本。技术研发人员:李玲,聂晶,梅享林,刘欢,王烨婷,吴其玉,吴欢,魏嫣受保护的技术使用者:湖北省医疗器械质量监督检验研究院技术研发日:技术公布日:2024/10/17本文地址:https://www.jishuxx.com/zhuanli/20241021/320413.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
上一篇
生产RNA的方法与流程
下一篇
返回列表