一种多策略提升全细胞微生物传感器性能的方法
- 国知局
- 2024-06-20 10:44:39
本发明属于生物,具体涉及一种基于抗性基因及适应性实验室进化技术的多策略提升全细胞微生物传感器性能的方法。
背景技术:
1、全细胞微生物传感器利用微生物细胞作为感知工具,感知环境和医学样品中的目标化学物质,并在原位控制细胞的代谢和行为。这种传感器成本低、易于使用且便携。在全细胞微生物传感器中,转录因子(transcription factor,tf)为基础的生物传感器得到广泛研究和应用。一般而言,生物传感器包括一个对目标配体敏感的转录调控因子(transcriptional factor,tf)、其配对的dna启动子和一个报告基因(例如红色荧光蛋白(red fluorescence protein,rfp))。tf是关键组成部分,它与其特定配体结合并发生构象变化,然后激活或抑制其与dna启动子的结合,进而调节后续执行器基因的表达。这些生物传感器已广泛应用于监测重金属和有机化学物质(如hg2+、ni2+、酚和羟基戊二酸)、环境生物修复以及生物生产中的动态控制。
2、适应性实验室进化(adaptive laboratory evolution,ale)是一种强大且易于使用的获得所需微生物的方法,尤其适用于生成对有毒化学物质耐受性更强的进化微生物。实验室进化模仿自然选择,通过在含有特定有毒化学物质的培养基中连续传代来富集耐受性微生物。这种生长耦合策略增强了细胞对高浓度有毒化学物质(甚至是抗生素)的耐受性。进化后的微生物获得有益的基因突变,以适应恶劣的条件。ale具有操作简便、高通量、无需基因背景和细胞工具、高效率获得所需特性的微生物等优点,已在学术界和工业界得到广泛应用。
3、目前全细胞微生物传感器适用于生物可利用性样品,但不适用于有毒抗生素,特别是在相对高的浓度下。当暴露于有毒化学物质时,全细胞微生物传感器在原位控制和监测方面效果不佳。优化基于tf的生物传感器用于抗生素是具有挑战性的,需要一种新的策略。
4、四环素(tetracycline,tc)是一种广为人知且广泛用于治疗人类和动物各种感染的抗生素。它被用作人类和兽医药物,以及动物生长促进剂。tc由一些放线菌产生,其活性谱涵盖广谱的革兰氏阴性和革兰氏阳性细菌,甚至原虫寄生虫。乳酸链球菌素(nisin)是一种由一些革兰氏阳性细菌产生的34个氨基酸残基组成的细菌素。nisin是许多国家批准用作食品防腐剂的唯一抗菌肽,因为它在人体中的毒性极小。nisin和tc都是抗菌剂,对宿主细胞有毒。但是,tc和nisin全细胞微生物传感器,在相对较高浓度的相应配体下都不能很好地工作。
5、请参见图1至图3,构建一个常见的无水四环素(四环素衍生物)生物传感器并用于在野生型(wild type,wt)大肠杆菌(escherichia coli,e.coli)中测试,该传感器质粒pb2c-gfp由tf tetr、其同源启动子ptet和gfp报告基因组成。该生物传感器仅在相对较低的tc浓度范围内(0至200nm)起作用(图2和3),这与先前报道的数据一致。然而,生物传感器对>200nm tc的荧光响应(图2)及其相应的细胞生长速率(图3)急剧减少。由于tc的毒性,tc浓度较高(>2,000nm)时大肠杆菌株几乎不生长。
6、请参见图4至图6,构建一个nisin生物传感器质粒,使用可以响应nisin的质粒pnz8148,该质粒是大肠杆菌和乳酸菌的穿梭载体。在nisin诱导启动子pnis的3’末端插入了一个rfp基因,然后对其相关的rbs进行了优化,将原始rbs序列5'-aaggaggcactcacc-3'替换为5'-tctagatgattaactttata aggaggaaaaacat-3’,以避免表达额外的小肽,生成nisin生物传感器质粒pnz8148-pnisrfp。采用野生型(wt)lactococcus lactis(l.lactis)nz9000作为宿主菌株,其含有响应nisin的双组分调控系统nisrk(图4)。pnz8148-pnisrfp被引入nz9000菌株,形成nisin全细胞微生物传感器(sensor-nis-wt)。生物传感器在0-20ng·ml-1nisin浓度范围内表现良好,但在高于20ngml-1nisin浓度下,细胞生长和生物传感器性能显著减少(图5和6)。
7、也就是说,对于含有高抗生素含量的样本必须适当稀释到适合全细胞微生物传感器检测的范围。然而,在一些情况下,如动态控制和原位监测,稀释和提取是不可能的。
8、因此,有必要研发一种提升全细胞微生物传感器的方法,以满足含有高抗生素含量的样本的检测需求。
技术实现思路
1、针对现有技术中的不足之处,本发明提供一种多策略提升全细胞微生物传感器性能的方法,从而让生物全细胞微生物传感器用于高效检测有毒化学物质或抗生素类化合物。
2、为了达到上述目的,本发明技术方案如下:
3、一种多策略提升全细胞微生物传感器性能的方法,包括两种策略:
4、策略一,向全细胞微生物传感器的宿主细胞内引入针对待检测物的抗性基因,以减少所述微生物的细胞内所述待检测物的浓度,所述待检测物包括抗生素和有毒化学物质,所述抗性基因包括但不限于待检测物外排泵编码基因、待检测物免疫蛋白编码基因、待检测物降解酶编码基因中的一种或几种,具体包括:
5、对于nisin生物传感器,分别选择引入nisin免疫蛋白编码基因nisi、nisin免疫相关abc转运蛋白编码基因nisfeg及nisin耐药降解酶编码基因nsr;引入nisi基因,构建了质粒pnz8148-pnisarfp/nisi,并在nisin生物传感器细胞l.lactis nz9000中表达,形成sensor-pnisarfp/nisi菌株;引入nisfeg基因,构建了质粒pnz8148-pnisarfp/nisefg,并在nisin生物传感器细胞l.lactis nz9000中表达,形成sensor-pnisarfp/nisefg菌株;引入nsr基因,构建了质粒pnz8148-pnisrfplnsr并在nisin生物传感器细胞l.lactis nz9000中表达,形成sensor-pnisrfp/nsr菌株;
6、对于链霉素生物传感器,引入转运蛋白编码基因strv、strw;
7、对于庆大霉素生物传感器,引入转运蛋白编码基因gnto;
8、对于卡那霉素生物传感器,引入转运蛋白编码基因kanj、kano、kanq、kanr、kans;
9、对于金霉素生物传感器,引入转运蛋白编码基因ctcr、ctcy、ctc2;
10、对于氯霉素生物传感器,引入转运蛋白编码基因cmlf、cmln;
11、对于克罗霉素生物传感器,引入转运蛋白编码基因kirti、kirtii;
12、对于螺旋霉素生物传感器,引入转运蛋白编码基因srmb;
13、对于林可霉素生物传感器,引入转运蛋白编码基因lmra、lmrc;
14、对于利福霉素生物传感器,引入转运蛋白编码基因rifp;
15、对于板霉素生物传感器,引入转运蛋白编码基因ptmp4;
16、对于枯草杆菌素生物传感器,分别引入枯草杆菌素免疫蛋白编码基因spai及枯草杆菌素免疫相关abc转运蛋白编码基因spafeg。
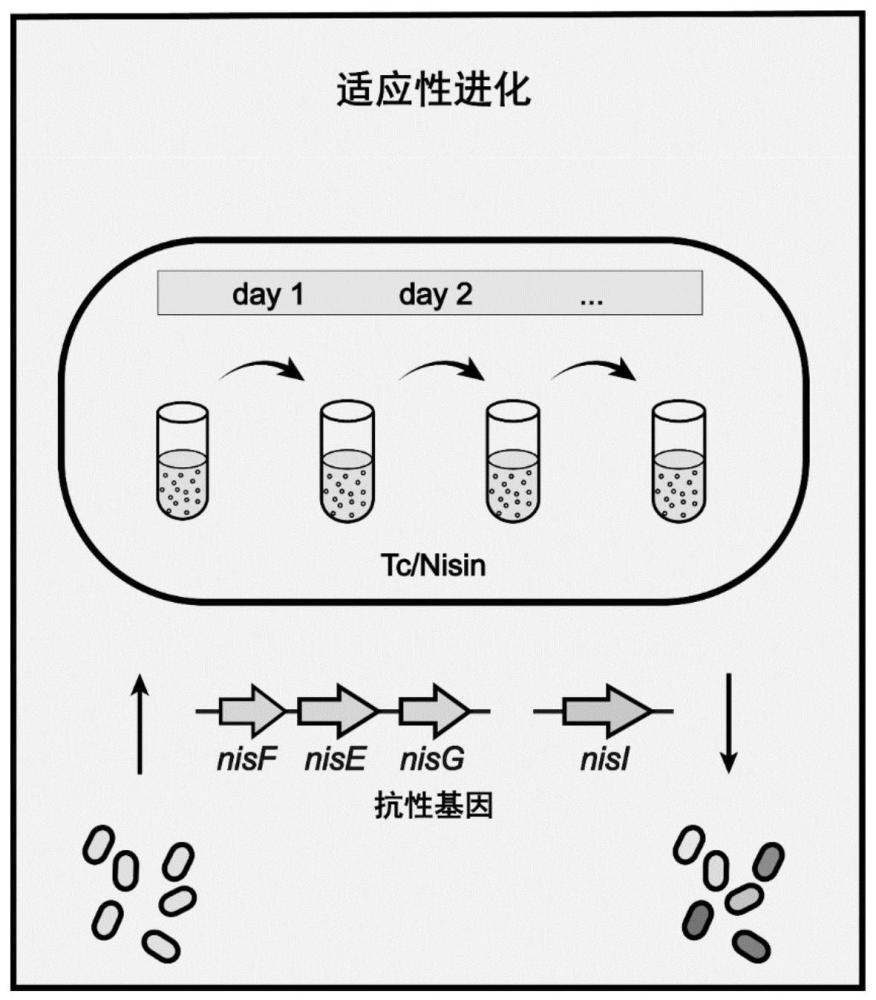
17、策略二,通过适应性实验室进化技术对所述宿主细胞进行进化,以提升所述宿主细胞的抗生素耐受性有毒化学物质耐受性,具体包括:
18、使用tc对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
19、使用nisin对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
20、使用链霉素对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
21、使用庆大霉素对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
22、使用卡那霉素对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
23、使用金霉素对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
24、使用氯霉素对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
25、使用克罗霉素对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
26、使用螺旋霉素对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
27、使用林可霉素对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
28、使用利福霉素对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
29、使用板霉素对e.coli菌株进行ale训练,从而获得具有耐受性的ale突变体作为宿主细胞;
30、使用枯草杆菌素对e.coli菌株进行ale训练,从而获得具有耐受性的al e突变体作为宿主细胞。
31、本发明的有益效果在于:
32、本发明采取了两种可选的策略以提升全细胞微生物传感器性能,通过引入待检测物的抗性基因以减少细胞内抗生素或有毒物质的浓度,或通过使用适应性实验室进化技术获得高耐受性的突变体构建新型生物传感器,从而实现对特定抗生素等毒性化学物质的稳定和高性能检测,此方法有助于开发适用于任何抗生素或有毒化学物质的全细胞微生物传感器,具有广泛的适用性。
33、上述说明仅是本发明技术方案的概述,为了能够更清楚了解本发明的技术手段,并可依照说明书的内容予以实施,以下以本发明的较佳实施例并配合附图详细说明如后。
本文地址:https://www.jishuxx.com/zhuanli/20240619/237.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表