一种耐药基因检测方法及系统与流程
- 国知局
- 2024-09-11 14:53:41
本发明涉及基因检测,具体而言,涉及一种耐药基因检测方法及系统。
背景技术:
1、抗生素的大量使用,导致细菌通过获得基因或染色体突变,使之能够耐受这些药物,从而产生细菌耐药性,使得多种传染病可能没有可行的抗生素治疗,对人类健康造成巨大的风险。细菌耐药性已成为威胁全球公共卫生健康的重要因素之一。2017年世界卫生组织(world health organization,who)发布对人类健康最具威胁的12种“超级细菌”,表明细菌抗生素耐药性已成为全球公共卫生问题。
2、根据我国2014至2019年及2022上半年的细菌耐药性监测报告显示,耐药性大肠埃希菌、肺炎克雷伯菌、金黄色葡萄球菌、铜绿假单胞菌和鲍曼不动杆菌为我国临床主要耐药菌。其中除金黄色葡萄球菌外均为革兰氏阴性菌。我国临床分离肺炎克雷伯菌对碳青霉烯类抗菌药物的耐药率从2005年的3%快速攀升至2019年的25%以上,上升幅度高达8倍。2018年全国细菌耐药监测网(carss)数据显示,全国1429所医院临床分离的肺炎克雷伯菌对碳青霉烯类抗菌药物的平均耐药率为10.1%,部分省市甚至超过20%。
3、基于细菌的耐药基因检测技术,目前已有商业化产品应用到了临床,如unyvero在对呼吸道常见病原体鉴定的同时纳入10种耐药基因为临床用药提供指导,有助于提高呼吸机相关性肺炎(icu vap)与医院获得相关性肺炎(hap)患者的早期精准诊断并减少广谱抗生素的使用;xpert carba-r assay可以检测四种碳青霉烯耐药基因(kpc,ndm,vim,imp,and oxa-48);最新升级的filmarray的血培养鉴定panel包含了11种常见的耐药基因。
4、然而,传统细菌耐药性检测方法虽能提供细菌耐药的表型信息,但需要长时间的培养和鉴定,且无法检测耐药基因;因此,本发明提出了一种耐药基因检测方法及系统,以至少部分解决现有技术中可能存在的问题。
技术实现思路
1、本发明的目的在于提供一种耐药基因检测方法及系统,其能够针对现有技术的不足,提出解决方案,以至少部分解决现有技术中可能存在的问题。
2、为解决上述技术问题,本发明采用的技术方案为:
3、一种耐药基因检测方法,包括:
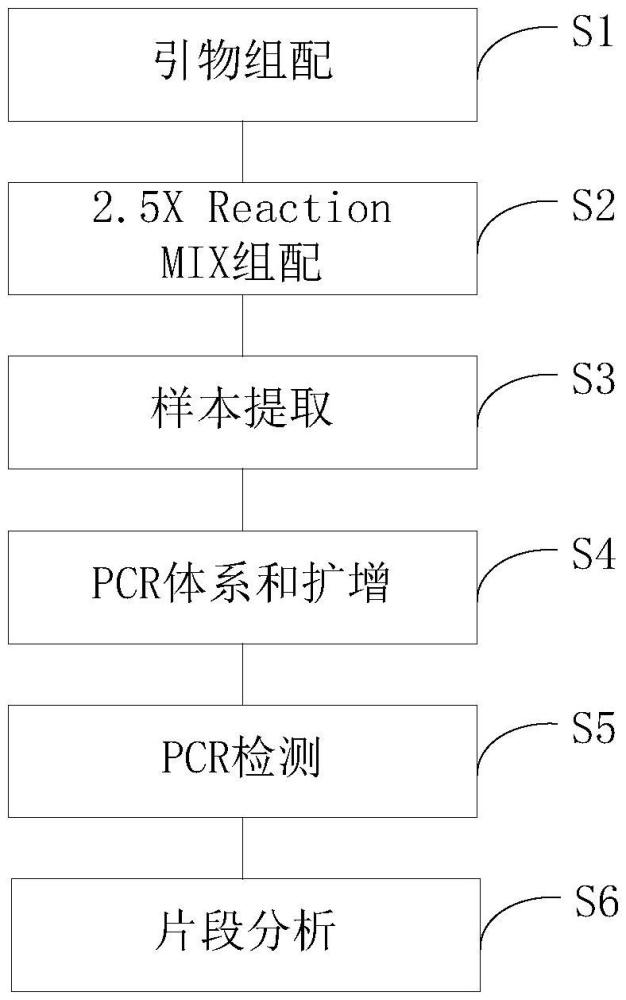
4、引物组配:按照预设基因序列参数表,将由hplc纯化后,且纯度至少为95%的引物,组配成5x引物混合物;
5、2.5x reaction mix组配:按照预设比例将缓冲液、化学盐、有机物助剂以及dna聚合酶混合组成2.5x反应组合物;
6、样本提取:获取灭活后的菌株浓度为100cfu/ml的混合检测样本,并分别进行10倍、100倍以及1000倍稀释,再通过buffer ave试剂洗脱,获得1000cfu/ml,100cfu/ml和10cfu/ml三种浓度混合菌液的样本dna;
7、pcr体系和扩增:将所述5x引物混合物、所述2.5x反应组合物以及所述样本dna按预设配置表配置,并按照预设次序循环扩增反应,获得pcr产物;
8、pcr检测:将预先处理好的荧光染色剂与所述pcr产物进行混合,并依次通过加热变性第一预设时长,冰浴第二预设时长,以及通过基因测序仪进行电泳检测,获得检测结果;
9、片段分析:通过片段分析软件,基于检测结果的检测峰和样本的扩增峰相对的降低情况,确定是否检出耐药基因。
10、可选地,所述按照预设基因序列参数表,将由hplc纯化后,且纯度至少为95%的引物,组配成5x引物混合物,包括:
11、获取包括kpc基因,vim基因,ndm基因,oxa-23基因,oxa-24基因,oxa-48基因,oxa-58基因,oxa-163基因、imp基因、ctx-m基因、tem基因、meca基因和mcr-基因的13个耐药基因序列模板;
12、从基因序列参数表中,获得序列genebank号与基因系列进行比对,确定所述基因系列的保守区域和突变区域,并选择其中最保守的区域确定引物,以及通过hplc纯化所述引物,获得纯度至少为95%的引物;
13、按照预设的13个耐药基因检测引物和内参引物表,确定引物系列和浓度,以及所述基因序列的扩增物大小的对应关系;
14、根据所述对应系和纯化后的所述引物进行配置得到5x引物混合物。
15、可选地,所述按照预设比例将缓冲液、化学盐、有机物助剂以及dna聚合酶混合组成2.5x反应组合物,包括:
16、按照如下组分配置:125mm的tricine-koh在25℃时其ph值为8.8、100mm的kcl、40mm的(nh4)2so4、6mm的mgcl2、1.2mm的dntps、2.5mm的dtt、2.5mg/ml的bsa、1m浓度为1%~20%的甜菜碱以及0.25u/μl的dna聚合酶,进行混合制得2.5x反应组合物。
17、可选地,所述获取灭活后的菌株浓度为100cfu/ml的混合检测样本,并分别进行10倍、100倍以及1000倍稀释,再通过buffer ave试剂洗脱,获得1000cfu/ml,100cfu/ml和10cfu/ml三种浓度混合菌液的样本dna,包括:
18、在基于ngs验证含耐药基因的菌中,每种耐药基因各选择一株,取各种菌液1000cfu,配置成一定量的混合菌液;
19、对所述混合菌液进行灭活处理,并至少分为三份,分别进行10倍、100倍以及1000倍稀释;
20、将稀释后的每份所述混合菌液,通过qiaamp minelute virus spin kit试剂进行提取,再以50μl的buffer ave试剂洗脱,获得1000cfu/ml,100cfu/ml和10cfu/ml三种浓度混合菌液的样本dna。
21、从ngs(二代测序技术)验证含耐药基因的菌中,每种耐药基因各选择一株,取各种菌液1000cfu,配置成1ml混合菌液。样本由某省疾控中心惠赠,灭活后混合成检测样本,每种菌株浓度为100cfu/ml。对混好的样本,分别稀释10倍,100倍,经qiaamp minelute virusspin kit(货号57704,qiagen)提取,按说明书操作,最后以50μl微升buffer ave洗脱。获得1000cfu/ml,100cfu/ml和10cfu/ml三种浓度混合菌液的提取dna。
22、可选地,所述将所述5x引物混合物、所述2.5x反应组合物以及所述样本dna按预设配置表配置,并按照预设次序循环扩增反应,获得pcr产物,包括:
23、将所述5x引物混合物、所述2.5x反应组合物以及所述样本dna按预设配置表进行混合配置,通过95℃环境下预变性处理2min;
24、将预变性处理后的混合物,依次通过94℃持续10s,54℃~64℃持续30s以及72℃持续30s,进行热循环处理至少30次,获得第一扩增产物;
25、将所述第一扩增产物,在60℃下持续或者54℃~64℃阶梯式进行2min的终延伸处理,获得pcr产物。
26、可选地,所述将预变性处理后的混合物,依次通过94℃持续10s,54℃~64℃持续30s以及72℃持续30s,进行热循环处理至少30次,获得第一扩增产物,包括:
27、所述将预变性处理后的混合物,依次通过94℃持续10s,以54℃、54℃、56℃、58℃、60℃、62℃、64℃阶梯式升温持续30s,以及72℃持续30s,进行热循环处理30~32次,获得第一扩增产物。
28、可选地,还包括对所述pcr产物在4℃的恒温下进行保藏。
29、可选地,所述将预选处理好的荧光染色剂与所述pcr产物进行混合,并依次通过加热变性第一预设时长,冰浴第二预设时长,以及通过基因测序仪进行电泳检测,获得检测结果,包括:s5
30、由去离子甲酰胺与liz-120荧光染色剂进行混合,获得荧光混合物;
31、将12.5ul剂量的所述荧光混合物和1ul的pcr产物进行混合,并去除其中的气泡,得到混合有荧光剂的pcr产物;
32、将混合有荧光剂的pcr产物,在95℃的环境中进行变性处理3min;
33、在变性处理后,进行3min的冰浴处理;
34、通过一代基因测序仪,对冰浴处理后的产物,进行电泳检测,获得检测结果。
35、可选地,所述通过片段分析软件,基于检测结果的检测峰和样本的扩增峰相对的降低情况,确定是否检出耐药基因,包括:s6
36、使用片段分析软件genemapper和遗传分析仪对所述检测结果进行检测分析;
37、依据检测1000cfu/ml、100cfu/ml和10cfu/ml三种浓度混合菌液样本和三种浓度混合样本中的13个耐药基因及内参均的扩增峰进行分析,当样本稀释后检测峰相对于所述扩增峰有明显降低,确定全部耐药基因均检出。
38、一种耐药基因检测系统,所述装置用于实现上述的耐药基因检测方法;所述装置包括:
39、引物组配模块:按照预设基因序列参数表,将由hplc纯化后,且纯度至少为95%的引物,组配成5x引物混合物;
40、2.5x reaction mix组配模块:按照预设比例将缓冲液、化学盐、有机物助剂以及dna聚合酶混合组成2.5x反应组合物;
41、样本提取模块:获取灭活后的菌株浓度为100cfu/ml的混合检测样本,并分别进行10倍、100倍以及1000倍稀释,再通过buffer ave试剂洗脱,获得1000cfu/ml,100cfu/ml和10cfu/ml三种浓度混合菌液的样本dna;
42、pcr体系和扩增模块:将所述5x引物混合物、所述2.5x反应组合物以及所述样本dna按预设配置表配置,并按照预设次序循环扩增反应,获得pcr产物;
43、pcr检测模块:将预先处理好的荧光染色剂与所述pcr产物进行混合,并依次通过加热变性第一预设时长,冰浴第二预设时长,以及通过基因测序仪进行电泳检测,获得检测结果;
44、片段分析模块:通过片段分析软件,基于检测结果的检测峰和样本的扩增峰相对的降低情况,确定是否检出耐药基因。
45、本发明至少具有如下优点或有益效果:
46、通过引物组配:按照预设基因序列参数表,将由hplc纯化后,且纯度至少为95%的引物,组配成5x引物混合物;2.5x reaction mix组配:按照预设比例将缓冲液、化学盐、有机物助剂以及dna聚合酶混合组成2.5x反应组合物;样本提取:获取灭活后的菌株浓度为100cfu/ml的混合检测样本,并分别进行10倍、100倍以及1000倍稀释,再通过buffer ave试剂洗脱,获得1000cfu/ml,100cfu/ml和10cfu/ml三种浓度混合菌液的样本dna;pcr体系和扩增:将所述5x引物混合物、所述2.5x反应组合物以及所述样本dna按预设配置表配置,并按照预设次序循环扩增反应,获得pcr产物;pcr检测:将预先处理好的荧光染色剂与所述pcr产物进行混合,并依次通过加热变性第一预设时长,冰浴第二预设时长,以及通过基因测序仪进行电泳检测,获得检测结果;片段分析:通过片段分析软件,基于检测结果的检测峰和样本的扩增峰相对的降低情况,确定是否检出耐药基因。解决了传统细菌耐药性检测方法虽能提供细菌耐药的表型信息,需要长时间的培养和鉴定,且无法检测耐药基因的问题,突破现有技术的限制,可以在不进行长时间培养和鉴定的情况下,进行检测耐药基因,实现高效快速检测。
本文地址:https://www.jishuxx.com/zhuanli/20240911/292483.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表