一种三维血管化心肌组织的制备方法及其应用
- 国知局
- 2024-12-06 12:27:44
本发明涉及生物技术,具体涉及一种三维血管化心肌组织的制备方法及其应用。
背景技术:
1、心肌梗死每年会造成全世界数百万人的死亡。新兴的心脏组织工程技术能够通过重建和替换坏死的心肌组织以恢复其部分或全部功能,为克服此临床难题的提供可能性。目前,建立血管网络是心脏组织工程领域内的主要挑战之一,因为在体外培养或构建的心肌组织中,如果要使心肌细胞保持活力和功能,则需要在100-200μm范围内集成能够正常工作的功能性脉管系统。组织良好的血管网络可以确保工程组织氧气和营养物质的充足输送,这是维持细胞活力和器官特异性功能的先决条件。心脏特异性脉管系统的形成能够促进器官发育和功能成熟。人类的正常心脏具有十分致密的血管网络,心肌梗死后,梗死区的心肌组织会出现严重缺血缺氧的恶劣微环境,而现有技术中植入式工程心肌组织的微血管密度远远低于原生心脏。
2、血管类器官与其他类型的组织细胞能够形成器官或组织特异性脉管系统。本发明的研究人员发现,血管类器官中的血管细胞具有旁分泌功能,可以产生vegf、fgf-2等因子,这些因子可以用于抑制心肌细胞凋亡,促进血管新生,改善心梗区的恶劣微环境。因此,本发明预期通过血管类器官与心肌组织细胞的结合得到心肌组织,解决目前存在的植入式工程心肌组织的微血管密度远远低于原生心脏的问题。
3、在血管类器官模型构建过程中,基质凝胶的添加必不可少。基质凝胶又称为脱细胞基质材料,是细胞微环境的重要组成部分,在体内可以调节细胞的生存和功能状态,同时还能够为细胞和组织提供力学支撑作用。血管类器官模型构建过程中,基质凝胶能够被降解以允许内皮细胞(ecs)迁移和浸润到周围组织中,促血管生成因子也会刺激内皮细胞,导致负责胶原蛋白、明胶和纤连蛋白降解的基质金属蛋白酶上调。
4、现有技术中,血管类器官构建过程中使用的基质凝胶一般来自于肿瘤组织。然而,这种基质凝胶会引入与肿瘤相关的蛋白或者因子,这些肿瘤相关的蛋白以及病理性因子的表达会对血管类器官的培养产生不良影响,进而影响心肌组织的构建。
5、所以,需要减少肿瘤病理性基质凝胶对血管类器官培养的不良影响,以建立具有高密度血管网络的预血管化工程心肌组织。
技术实现思路
1、(一)要解决的技术问题
2、本发明的研究人员预期将血管类器官与心肌组织细胞进行结合得到心肌组织,以解决目前存在的植入式工程心肌组织的微血管密度远远低于原生心脏的问题。而在将血管类器官与心肌组织细胞进行结合的过程中,还需要解决现有技术中存在的肿瘤组织来源的基质凝胶对血管类器官培养以及血管化心肌组织构建的不良影响的问题,鉴于上述技术问题,本发明提供一种三维血管化心肌组织的制备方法及其应用。
3、(二)技术方案
4、为了达到上述目的,本发明采用的主要技术方案包括:
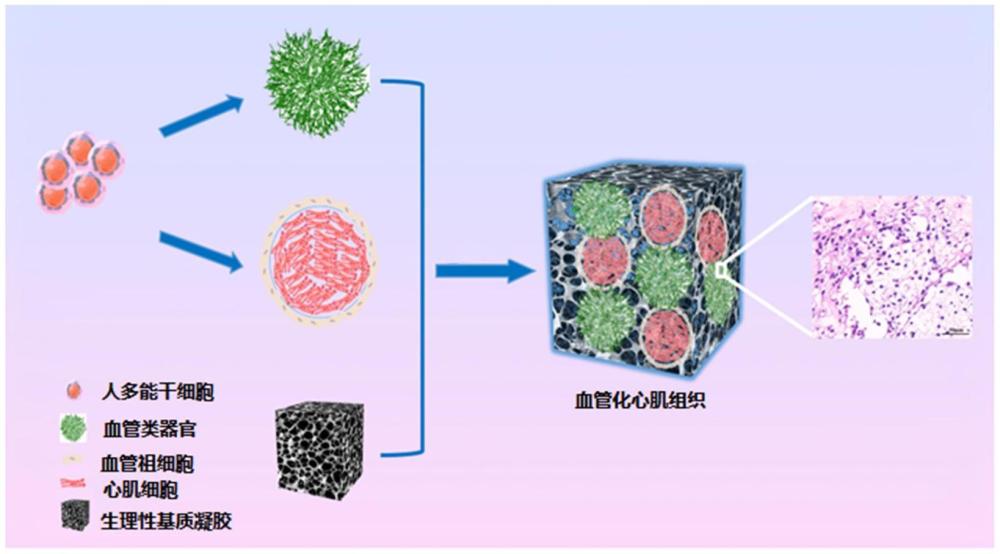
5、一种三维血管化心肌组织的制备方法,包括如下步骤:
6、s1:通过人源组织或者动物源组织制备生理性基质凝胶;
7、s2:通过人多能干细胞制备拟胚体,然后培养拟胚体,得到血管祖细胞球;
8、s3:将步骤s1制备得到的生理性基质凝胶铺设在孔板底部,孵育培养后得到第一层胶体,然后将步骤s2制备得到的血管祖细胞球和步骤s1制备得到的生理性基质凝胶混合后加入孔板中孵育培养,得到第二层胶体,接着向孔板加入培养基,培养得到血管网络或者血管类器官;
9、s4:通过心肌细胞制备心肌球,然后将步骤s2制备得到的血管祖细胞球经过消化处理后封装在心肌球的表面;或者,将心肌细胞封装在步骤s2制备得到的血管祖细胞球的表面;
10、s5:将步骤s3制备得到的血管网络以及步骤s4制备得到的表面封装血管祖细胞的心肌球包裹在步骤s1制备得到的生理性基质凝胶中,然后进行培养,得到三维血管化心肌组织;或者将步骤s3制备得到的血管类器官、心肌细胞以及步骤s4制备得到的表面封装心肌细胞的血管祖细胞球分散在步骤s1制备得到的生理性基质凝胶中,然后进行培养,得到三维血管化心肌组织。
11、如上所述的三维血管化心肌组织的制备方法,优选地,步骤s1中,所述人源组织为脐带华通胶、人的脾脏、小肠、肝脏、肺或者胃,所述动物源组织为动物的脾脏、小肠、肝脏、肺或者胃。
12、如上所述的三维血管化心肌组织的制备方法,优选地,步骤s1具体包括:
13、s11:去除人源组织或者动物源组织中的杂质,将其粉碎、漂洗后进行脱细胞处理,得到生理性基质组织块;
14、s12:清洗生理性基质组织块后对其进行真空冷冻干燥处理;
15、s13:称取冷冻干燥后的生理性基质组织块,加入酸性的胃蛋白酶进行酶消化处理,得到生理性基质溶液;
16、s14:对生理性基质溶液的ph进行调节,然后加入缓冲液,得到生理性基质凝胶。
17、如上所述的三维血管化心肌组织的制备方法,优选地,步骤s11中,去除人源组织或者动物源组织中的杂质后将其粉碎成1-3mm3的组织小块;
18、步骤s13中,向冷冻干燥后的生理性基质中加入缓冲液并研磨成匀浆,再加入酸性的胃蛋白酶进行酶消化处理,得到生理性基质溶液;
19、步骤s14中,向生理性基质溶液加入氢氧化钠溶液,将ph调节至7-8,然后加入磷酸盐缓冲液,得到生理性基质凝胶。
20、如上所述的三维血管化心肌组织的制备方法,优选地,步骤s2具体包括:
21、s21:对人多能干细胞进行消化处理,得到人多能干细胞的单细胞悬液;
22、s22:将步骤s21制备得到的单细胞悬液加入24微孔板模具中,再向每个微孔中加入含有蛋白因子rock-y27632的聚集培养基,此时记为第0天,培养24小时后得到拟胚体,然后将培养基更换为第一中胚层诱导培养基,此时记为第1天,此后每天更换培养基;
23、s23:在培养的第4-6天中,将培养基更换为血管诱导培养基,并且每天更换培养基,第6天得到大小均一的血管祖细胞球。
24、如上所述的三维血管化心肌组织的制备方法,优选地,步骤s3具体包括:
25、s31:在预冷的12孔板中加入300-500μl/孔的生理性基质凝胶,在37℃下孵育20min-40min,使孔板底部形成第一层胶体;
26、s32:将步骤s2制备得到的血管祖细胞球和步骤s1制备得到的生理性基质凝胶混合均匀,使每毫升生理性基质凝胶中含有30-50个血管祖细胞球,接着将血管祖细胞球与生理性基质凝胶的混合物加入孔板,使孔板的每个孔中含有20-30个血管祖细胞球血管祖细胞球/500μl生理性基质凝胶,然后使孔板在37℃下孵育60-120min,得到第二层胶体;
27、s33:向孔板中加入培养基,继续培养3-5天后得到血管网络,或者向孔板中加入培养基,继续培养7-9天后得到血管类器官。
28、如上所述的三维血管化心肌组织的制备方法,优选地,当步骤s3培养得到血管网络,步骤s4具体包括:
29、s41:获取心肌细胞,然后将心肌细胞制备成心肌悬液,向心肌悬液中加入生理性基质凝胶,混合均匀后将心肌悬液加入微孔培养板中,然后将微孔培养板放入细胞培养箱中孵育培养,得到心肌球;
30、s42:对步骤s2制备得到的血管祖细胞球进行消化处理,得到单细胞悬液,然后将单细胞悬液加入步骤s41经过孵育后的微孔培养板中,继续将微孔培养板放入细胞培养箱中孵育培养,得到表面封装血管祖细胞的心肌球;
31、当步骤s3培养得到血管类器官,步骤s4具体包括:
32、s41:获取心肌细胞,然后将心肌细胞制备成心肌悬液,将心肌悬液加入步骤s2制备得到的包含血管祖细胞球的微孔板中,得到表面封装心肌细胞的血管祖细胞球。
33、如上所述的三维血管化心肌组织的制备方法,优选地,步骤s41中的心肌细胞为人多能干细胞诱导分化得到的心肌细胞、动物体中提取得到的原代心肌细胞,或者从心脏类器官中提取得到的细胞。
34、如上所述的三维血管化心肌组织的制备方法,优选地,步骤s5具体包括:
35、s51:将步骤s1制备得到的生理性基质凝胶铺设在微孔培养板中微孔的底部;
36、s52:将步骤s3制备得到的血管网络以及步骤s4制备得到的表面封装血管祖细胞的心肌球混合,然后将混合物接种至步骤s51铺设的生理性基质凝胶上,然后孵育培养;或者将步骤s3制备得到的血管类器官、心肌细胞以及步骤s4制备得到的表面封装心肌细胞的血管祖细胞球混合,然后将混合物接种至步骤s51铺设的生理性基质凝胶上,然后孵育培养;
37、s53:向微孔培养板的孔中加入血管成熟培养基,每天更换培养基,对于血管网络与心肌球的混合物,加入血管成熟培养基后培养3-5天后得到三维血管化心肌组织;对于血管类器官与心肌细胞以及表面封装心肌细胞的血管祖细胞球的混合物,加入血管成熟培养基后培养3-5天后得到三维血管化心肌组织。
38、本发明还提供一种上述三维血管化心肌组织的制备方法的应用,所述三维血管化心肌组织的制备方法用于疾病模型的构建、类器官的血管化、再生医学以及药物筛选。
39、(三)有益效果
40、本发明首次通过人源组织/动物源组织制备生理性基质凝胶,并将其代替肿瘤来源的基质水凝胶,用于血管类器官以及三维血管化心肌组织的培养,能够减少肿瘤相关的蛋白或者因子的引入,使得血管类器官以及心肌组织所处的培养环境更接近人体生理性环境,避开肿瘤相关标志物对血管类器官培养以及心肌组织培养的干扰,使血管类器官在临床用用上得到进一步的改善和突破。另外,本发明所使用的人源组织/生理性基质凝胶还能够促进血管类器官的成熟,缩短血管类器官的培养时间。
41、本发明将血管类器官与心肌组织细胞进行结合,培养得到具有高度血管化结构的三维血管化心肌组织,且本发明制备得到的三维血管化心肌组织的厚度可以达到1mm,具有搏动的功能,更加接近人体正常心脏中心肌组织的发育程度,能够解决目前存在的植入式工程心肌组织的微血管密度远远低于原生心脏的问题。
本文地址:https://www.jishuxx.com/zhuanli/20241204/341512.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表