检测肠炎沙门氏菌的LAMP引物组合物及其试剂盒和方法
- 国知局
- 2024-08-05 11:55:30
本发明属于生物检测,具体涉及检测肠炎沙门氏菌的lamp引物组合物及其试剂盒和方法。
背景技术:
1、肠炎沙门氏菌(s.enteritidis)属于肠杆菌科沙门氏菌属肠道亚种肠炎血清型,是一种无芽孢,但有多个长鞭毛的革兰氏阴性菌。肠炎沙门氏菌具有广泛的宿主谱,能同时感染人类和各种动物,是一种具有重要公共卫生意义的疾病,主要引起腹泻、呕吐、脑膜炎、尿路感染等症状,严重者甚至死亡。动物食用被沙门氏菌污染的饲料是此类菌进入食物链的主要途径之一。肠炎沙门氏菌菌体抗原为o9,o12,鞭毛抗原为hm,hg,在显色二代培养基上呈深紫色菌落,可以发酵葡萄糖、麦芽糖、甘露醇。
2、常见的沙门氏菌检测方法主要有传统检测方法、分子生物学方法、免疫学检测方法等。传统培养方法(gb4789.4-2016)包括前增菌、选择性增菌、分离培养、生化试验和血清学鉴定等步骤,虽然传统检测方法准确度高,可重复性强,但这种检测方法操作复杂、无法进行现场检测、灵敏度低、检测周期长,一般要经过4-7天可以得到检测结果,无法实现对肠炎沙门氏菌的快速检测。
3、环介导等温扩增(loop-mediated isothermal amplification,lamp)是一种在恒温条件下连续的核酸体外扩增技术,该技术具有操作简单、特异性强、灵敏度高、检测时间短、产物易检测等优点,能够实现现场的快速检测,提高检测效率。但是采用该技术进行检测时需要找到特异性引物。
技术实现思路
1、本发明的目的是提供检测肠炎沙门氏菌的lamp引物组合物及其试剂盒和方法。
2、本发明提供了一种检测肠炎沙门氏菌的引物组合物,它是由seq id no:1~6所示的核苷酸序列组成。
3、进一步地,所述seq id no:1~2所示的核苷酸序列、seq id no:3~4所示的核苷酸序列和seq id no:5~6所示的核苷酸序列的摩尔比为1:(1~5):(1~5);
4、优选地,所述seq id no:1~2所示的核苷酸序列、seq id no:3~4所示的核苷酸序列和seq id no:5~6所示的核苷酸序列的摩尔比为1:4:2。
5、进一步地,所述seq id no:1和seq id no:2所示的核苷酸序列的摩尔比为1:1;所述seq id no:3和seq id no:4所示的核苷酸序列的摩尔比为1:1;所述seq id no:5和seqid no:6所示的核苷酸序列的摩尔比为1:1。
6、进一步地,所述检测肠炎沙门氏菌的方法为环介导等温扩增检测方法。
7、本发明还提供了前述的引物组合物在制备检测肠炎沙门氏菌的试剂盒中的用途;
8、优选地,所述试剂盒为环介导等温扩增检测用试剂盒。
9、本发明还提供了一种检测肠炎沙门氏菌的试剂盒,所述试剂盒中包含前述的引物组合物;
10、优选地,所述试剂盒为环介导等温扩增检测用试剂盒。
11、本发明还提供了一种检测肠炎沙门氏菌的方法,它包括如下步骤:
12、(1)从样品中提取dna;
13、(2)取步骤(1)提取得到的dna,加入用于环介导等温扩增的反应液中混合,建立扩增体系,并在60℃-65℃恒温条件下进行环介导等温扩增;所述反应液中包括前述的引物组合物;
14、(3)将荧光染料加入步骤(2)得到的扩增产物中,利用恒温荧光检测仪检测。
15、进一步地,
16、步骤(2)中,所述反应液每25μl包括ddh2o 3μl、引物混合物14μl、bst聚合酶mix 1μl、dna模板1μl、bst buffer 6μl;
17、和/或,步骤(3)中,所述荧光染料为sybr green;
18、和/或,步骤(3)中,所述恒温荧光检测仪的参数设置为:时间60min,检测间隔30s,温度65℃,阀值设置3-6min,方差倍数10。
19、进一步地,所述的引物混合物浓度为2.8mm,荧光染料浓度为5mm。
20、进一步地,所述环介导等温扩增程序为65℃扩增1h。
21、与现有技术相比,本发明的优势为:
22、(1)本发明采用环介导等温扩增(loop-mediated isothermal ampli-fication,lamp)技术,依赖于能够识别糖苷水解酶家族1蛋白(glycoside hydrolase family1protein)序列上6个特异区域的引物和一种具解旋功能且使靶序列呈环介导等温扩增的bst dna聚合酶,在等温条件下可高效、快速、特异地扩增靶序列。
23、(2)本发明提供的技术方案采用lamp扩增方式为环介导等温扩增,扩增效率高,由于lamp识别的是核酸上的6个特异性的位点,所以其特异性强。
24、(3)本发明提供的技术方案lamp只在60℃-65℃进行恒温扩增,过程只需水浴锅即可,也不需要特殊的仪器,因此非常简便;且由于lamp是恒温扩增,不需要反转录步骤及pcr仪升降温的时间,所以扩增时间短。
25、(4)本发明提供的技术方案lamp反应中加入荧光物质后,合成大量的dna时,在荧光恒温扩增仪器上可以看到扩增曲线,扩增过程一目了然。
26、(5)本发明提供的技术方案设计特异性引物,多细菌验证此方法的特异性,对lamp技术检测值与pcr检测值进行了比较,检验了其重复性与稳定性,建立了适用于现场检测肠炎沙门氏菌的快速检测方法。
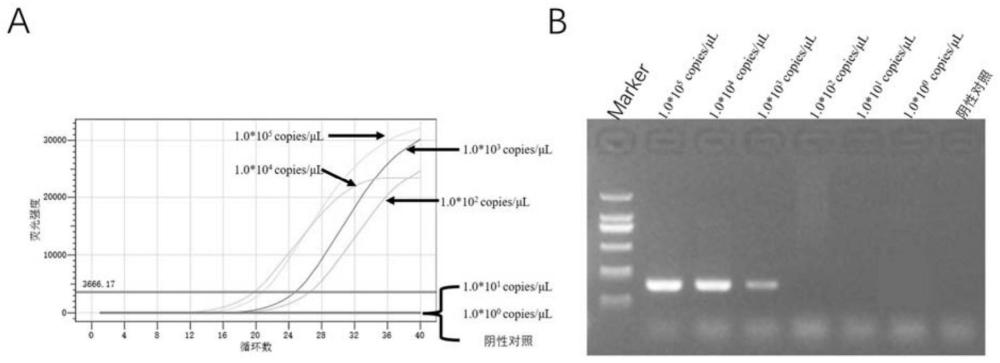
27、(6)本发明提供的技术方案lamp反应中加入100-105cfu/ml10倍稀释的菌液,敏感性为1cfu/ml,与pcr方法进行比较,敏感性优于普通pcr方法。
28、综上,本发明提供了一种检测肠炎沙门氏菌的lamp引物组合物,采用本发明引物组合物进行lamp检测肠炎沙门氏菌灵敏度高、特异性好、准确率高,并且该检测方法重复性和稳定性好。与pcr相比,检测效果显著提高。采用本发明lamp引物组合物检测肠炎沙门氏菌简便且速度快,适用于现场快速检测,具有良好的应用前景。
29、显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
30、以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
技术特征:1.一种检测肠炎沙门氏菌的引物组合物,其特征在于:它是由seq id no:1~6所示的核苷酸序列组成。
2.根据权利要求1所述的引物组合物,其特征在于:所述seq id no:1~2所示的核苷酸序列、seq id no:3~4所示的核苷酸序列和seq id no:5~6所示的核苷酸序列的摩尔比为1:(1~5):(1~5);
3.根据权利要求2所述的引物组合物,其特征在于:所述seq id no:1和seq id no:2所示的核苷酸序列的摩尔比为1:1;所述seq id no:3和seq id no:4所示的核苷酸序列的摩尔比为1:1;所述seq id no:5和seq id no:6所示的核苷酸序列的摩尔比为1:1。
4.根据权利要求1~3任一项所述的引物组合物,其特征在于:所述检测肠炎沙门氏菌的方法为环介导等温扩增检测方法。
5.权利要求1~4任一项所述的引物组合物在制备检测肠炎沙门氏菌的试剂盒中的用途;
6.一种检测肠炎沙门氏菌的试剂盒,其特征在于:所述试剂盒中包含权利要求1~4任一项所述的引物组合物;
7.一种检测肠炎沙门氏菌的方法,其特征在于:它包括如下步骤:
8.根据权利要求7所述的方法,其特征在于:
9.根据权利要求8所述的方法,其特征在于:所述的引物混合物浓度为2.8mm,荧光染料浓度为5mm。
10.根据权利要求7所述的方法,其特征在于:所述环介导等温扩增程序为65℃扩增1h。
技术总结本发明提供了检测肠炎沙门氏菌的LAMP引物组合物及其试剂盒和方法,属于生物检测技术领域。本发明引物组合物是由SEQ ID NO:1~6所示的核苷酸序列组成。本发明还提供了一种包含该引物组合物的试剂盒以及检测肠炎沙门氏菌的方法。采用本发明引物组合物进行LAMP检测肠炎沙门氏菌灵敏度高、特异性好、准确率高,并且该检测方法重复性和稳定性好。与PCR相比,检测效果显著提高。采用本发明LAMP引物组合物检测肠炎沙门氏菌简便且速度快,适用于现场快速检测,具有良好的应用前景。技术研发人员:胡晓亮,田志革,潘青,付巍,李琰,戚颖受保护的技术使用者:宜宾学院技术研发日:技术公布日:2024/8/1本文地址:https://www.jishuxx.com/zhuanli/20240802/260131.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表