生物标志物在制备预测肾透明细胞癌患者预后的产品中的应用
- 国知局
- 2024-08-05 11:53:13
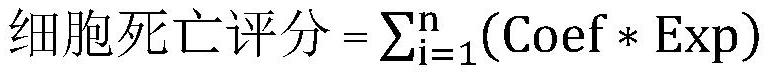
本发明涉及生物医学领域,更具体的是生物标志物在制备预测肾透明细胞癌患者预后的产品中的应用。
背景技术:
1、肾透明细胞癌(ccrcc或称kirc)是肾癌最常见的病理亚型。近年来,尽管有许多靶点被用于治疗肾透明细胞癌。然而,ccrcc的长期预后仍然不容乐观。因此,探索一种更可靠的早期预测肾透明细胞癌的预后模型至关重要。
2、细胞死亡主要分为两类:坏死和程序性细胞死亡(pcd)。程序性细胞死亡(pcd)是一个主动死亡过程,它不仅发生在个体的正常发育过程中,也发生在异常的生理状态或疾病中。既往研究已经定义了几种不同类型的pcd,包括凋亡、自噬、坏死性凋亡、焦亡、铁死亡、失巢凋亡、线粒体自噬、铜死亡等。不同形式的细胞死亡是相互关联的,并且是一个协调的系统。当任一通路发生缺陷时,会触发其他通路来执行细胞死亡过程。pcd通路功能障碍与肿瘤的发生和发展有关。
3、pink1(pten诱导激酶1)可以保护细胞免受压力引起的线粒体功能障碍。akr1c1(醛酮还原酶家族1成员c1)是醛/酮还原酶超家族的成员之一,通过利用nadh和/或nadph作为辅助因子来催化醛和酮转化为相应的醇。eif4ebp1(真核翻译起始因子4e结合蛋白1)被磷酸化后可响应各种信号(包括紫外线照射和胰岛素信号传导),导致其与eif4e解离并激活mrna翻译。psat1(磷酸丝氨酸转氨酶1)催化磷酸丝氨酸生成,是丝氨酸从头合成代谢的重要催化酶之一。chac1(chac谷胱甘肽特异性γ-谷氨酰环转移酶1)是一个新鉴定的内质网诱导基因,能够诱导细胞凋亡和铁死亡。cxcl2(cxc趋化因子配体2)是cxc趋化因子家族的一员,参与免疫调节和炎症过程。irf9(干扰素调节因子9)是干扰素调节因子(irf)家族成员之一,在包括肿瘤发生和炎症在内的几个生物学过程中起着至关重要的作用。
技术实现思路
1、本发明所要解决的技术问题是如何对肾透明细胞癌患者进行预后预测。
2、为解决上述技术问题,本发明首先提供了生物标志物和/或检测上述生物标志物的物质在制备预测肾透明细胞癌患者预后的产品中的应用,上述生物标志物为pink1基因,akr1c1基因,eif4ebp1基因,psat1基因,chac1基因,cxcl2基因和irf9基因这7个基因。
3、上述pink1为pten诱导激酶1。上述pink1的氨基酸序列可为genbank accessionno.np_115785.1(update date 2022.12.27)。上述pink1基因的核苷酸序列可为genbankaccession no.nm_032409.3的第92-1837位(update date2022.12.17)。上述akr1c1为醛酮还原酶家族1成员c1。上述akr1c1的氨基酸序列可为genbank accession no.np_001344.2(update date 2022.9.18)。上述akr1c1基因的核苷酸序列可为genbank accessionno.nm_001353.6的第31-1002位(update date 2022.9.18)。上述eif4ebp1为真核翻译起始因子4e结合蛋白1。上述eif4ebp1的氨基酸序列可为genbank accession no.np_004086.1(update date 2022.9.23)。上述eif4ebp1基因的核苷酸序列可为genbank accessionno.nm_004095.4的第41-397位(update date 2022.9.23)。上述psat1为磷酸丝氨酸转氨酶1。上述psat1的氨基酸序列可为genbank accession no.np_478059.1(update date2022.12.14)。上述psat1基因的核苷酸序列可为genbank accession no.nm_058179.4的第87-1199位(update date 2022.12.14)。上述chac1为chac谷胱甘肽特异性γ-谷氨酰环转移酶1。上述chac1的氨基酸序列可为genbank accession no.np_077016.3(update date2022.10.23)。上述chac1基因的核苷酸序列可为genbank accession no.nm_024111.6的第114-782位(update date 2022.12.25)。上述cxcl2为cxc趋化因子配体2。上述cxcl2的氨基酸序列可为genbank accession no.np_002080.1(update date 2022.11.30)。上述cxcl2基因的核苷酸序列可为genbank accession no.nm_002089.4的第76-399位(update date2022.11.30)。上述irf9为干扰素调节因子9。上述irf9的氨基酸序列可为genbankaccession no.np_006075.3(update date 2022.11.20)。上述irf9基因的核苷酸序列可为genbank accession no.nm_006084.5的第76-1257位(update date 2022.11.20)。
4、上述应用中,上述物质可为下述任一种:
5、a1)用于检测上述7个基因的mrna表达水平的试剂;
6、a2)用于检测上述7个基因的蛋白质表达水平的试剂。
7、具体地,上述mrna表达水平是指在转录水平上检测基因转录的mrna的丰度;上述蛋白质表达水平是指在翻译水平上检测基因编码的蛋白质的丰度。
8、上述应用中,上述物质包括通过逆转录-聚合酶链反应、实时荧光定量pcr、转录组测序技术、northern blot、原位杂交技术、基因芯片技术、nanopore测序技术、pacbio测序技术、免疫印迹法、免疫组化法、免疫荧光法、放射免疫测定法、免疫共沉淀法、酶联免疫吸附试验、酶免疫测定法、流式细胞术、高效液相色谱法、毛细管凝胶电泳法、近红外光谱法、质谱法、免疫化学发光法、胶体金免疫技术、荧光免疫层析技术、表面等离子共振技术、免疫-pcr技术或生物素-亲和素技术检测上述生物标志物的试剂。
9、上述应用中,所述物质可为体外核酸扩增所述7个基因的试剂。所述体外核酸扩增技术可为聚合酶链式反应(pcr)、链替代扩增(sda)、连接酶链式反应(lcr)和依赖核酸序列的扩增(nasba)、滚环核酸扩增(rca)、环介导等温扩增(lamp)、重组酶聚合酶扩增技术(rpa)、依赖解旋酶的等温扩增技术(hda)或qβ复制技术。所述体外核酸扩增所述7个基因的试剂具体可为pcr扩增所述7个基因的引物对组合物,所述引物对组合物由pink1基因特异引物对,akr1c1基因特异引物对,eif4ebp1基因,psat1基因特异引物对,chac1基因特异引物对,cxcl2基因特异引物对和irf9基因特异引物对组成;所述pink1基因特异引物对由pink1-f和pink1-r组成,所述pink1-f是核苷酸序列为序列1的单链dna,所述pink1-r是核苷酸序列为序列2的单链dna。所述akr1c1基因特异引物对由akr1c1-f和akr1c1-r组成,所述akr1c1-f是核苷酸序列为序列3的单链dna,所述akr1c1-r是核苷酸序列为序列4的单链dna。所述eif4ebp1基因特异引物对由eif4ebp1-f和eif4ebp1-r组成,所述eif4ebp1-f是核苷酸序列为序列5的单链dna,所述eif4ebp1-r是核苷酸序列为序列6的单链dna。所述psat1基因特异引物对由psat1-f和psat1-r组成,所述psat1-f是核苷酸序列为序列7的单链dna,所述psat1-r是核苷酸序列为序列8的单链dna。所述chac1基因特异引物对由chac1-f和chac1-r组成,所述chac1-f是核苷酸序列为序列9的单链dna,所述chac1-r是核苷酸序列为序列10的单链dna。所述cxcl2基因特异引物对由cxcl2-f和cxcl2-r组成,所述cxcl2-f是核苷酸序列为序列11的单链dna,所述cxcl2-r是核苷酸序列为序列12的单链dna。所述irf9基因特异引物对由irf9-f和irf9-r组成,所述irf9-f是核苷酸序列为序列13的单链dna,所述irf9-r是核苷酸序列为序列14的单链dna。
10、上述应用中,上述产品可包括用于检测上述生物标志物的物质。
11、上述应用中,上述产品可包括试剂盒、基因芯片、蛋白质芯片、免疫层析诊断试纸、高通量测序平台或生物传感器。
12、上述应用中,上述产品的检测样本可为新鲜组织。
13、为解决上述技术问题,本发明还提供了预测肾透明细胞癌患者预后的产品。
14、本发明所提供的预测肾透明细胞癌患者预后的产品包括上述生物标志物和/或检测上述生物标志物的物质。
15、为解决上述技术问题,本发明还提供了预测肾透明细胞癌患者预后的装置。
16、本发明所提供的预测肾透明细胞癌患者预后的装置包括数据处理模块,上述数据处理模块用于根据待测肾透明细胞癌患者的上述7个基因表达水平对上述待测肾透明细胞癌患者进行预后评价。
17、上述装置还包括检测生物标志物的模块,上述模块用于检测待测肾透明细胞癌患者的上述7个基因表达水平。
18、上述装置中,上述数据处理模块根据公式1给出待测肾透明细胞癌患者的预后评分,根据上述预后评分对上述待测肾透明细胞癌患者进行预后评价;上述预后评分按照公式1计算,
19、公式1:
20、s=-0.36924×e1-0.12953×e2+0.129647×e3+0.154479×e4+0.160814×e5
21、+0.090451×e6+0.29436×e7
22、公式1中:
23、s为预后评分,
24、e1为pink1基因表达水平,
25、e2为akr1c1基因表达水平,
26、e3为eif4ebp1基因表达水平,
27、e4为psat1基因表达水平,
28、e5为chac1基因表达水平,
29、e6为cxcl2基因表达水平,
30、e7为irf9基因表达水平。
31、为解决上述技术问题,本发明还提供了存储有计算机程序的计算机可读存储介质。
32、本发明所提供的存储有计算机程序的计算机可读存储介质中上述计算机程序使计算机执行如下步骤:根据待测肾透明细胞癌患者的上述7个基因表达水平对肾透明细胞癌患者进行预后评价。
33、上述计算机可读存储介质中,计算机程序还可使计算机执行如下步骤:获取待测肾透明细胞癌患者的上述7个基因表达水平。
34、上述计算机可读存储介质中,上述计算机程序还可使计算机执行如下步骤:上述预后根据预后评分进行,上述预后评分按照公式1计算:
35、公式1:
36、s=-0.36924×e1-0.12953×e2+0.129647×e3+0.154479×e4+0.160814×e5
37、+0.090451×e6+0.29436×e7
38、公式1中:
39、s为预后评分,
40、e1为pink1基因表达水平,
41、e2为akr1c1基因表达水平,
42、e3为eif4ebp1基因表达水平,
43、e4为psat1基因表达水平,
44、e5为chac1基因表达水平,
45、e6为cxcl2基因表达水平,
46、e7为irf9基因表达水平。
47、实验证明:根据公式1对101名肾透明细胞癌患者进行预后评分,根据预后评分的中位值(阈值)将患者分为高危组(n=50)和低危组(n=51)。高危组患者的总生存率明显低于低危组患者(图5中d),两组患者之间的总生存率存在显著差异。在肾透明细胞癌患者中,利用风险评分对1、3和5年生存率预测的auc分别为0.758、0.732和0.782(图5中e)。
48、在kirc队列中,单因素cox回归分析结果表明:风险评分与os密切相关(hr:1.447,95%ci(1.342-1.561),p<0.001;图5中f)。校正临床特征后,多因素cox回归分析结果证实:高风险评分仍然是os的独立危险因素(hr:1.278,95%ci(1.174-1.392),p<0.001;图5中g)。基于多因素cox回归分析的结果,我们在kirc队列中构建了预测肾透明细胞癌患者预后的列线图(图5中h),一致性指数(c指数)值为0.772(95%ci:0.755–0.789),说明本发明的模型可以用于评估肾透明细胞癌患者的预后。
本文地址:https://www.jishuxx.com/zhuanli/20240802/259902.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。