组合物、制备多肽的偶联物的方法及偶联物
- 国知局
- 2024-10-21 14:59:51
本发明涉及一种利用包含奥沙宁的适体的多肽偶联物(conjugate)的制备。更具体而言,涉及一种用于制备包括包含奥沙宁的适体(aptamer)的多肽偶联物的组合物及利用此的多肽偶联物制备方法。此外,涉及一种包括包含奥沙宁的适体和多肽的偶联物,或包含药物和多肽的偶联物。本研究是在三星未来技术培育事业的支援下进行的(课题编号:srfc-ma2001-08)。
背景技术:
1、随着生物偶联物化学(bioconjugate chemistry)的多种技术的出现,生命工学领域的研究开发的模式正在急剧变化。通过将一个分子与另一个分子化学连接,可以制备将蛋白质、核酸(na)、脂质、碳水化物或其他生物活性分子乃至整个细胞等多种功能的分子成功结合的全新的生物活性偶联物分子。这种功能性整合具有很好的协同效果,例如,与细胞毒性药物单独作用的情况相比,在作为抗体-药物偶联物(adc:antibody-drug conjugate)起作用的情况下,药物的疗效可以进一步增加100-1000倍。实际上,由生物偶联物化学主导的技术发展在医疗和制药领域具有影响力,并创造了高附加值产业。在过去的10年期间,在肿瘤学市场有六种抗体-药物偶联物(adc)药物被批准并销售。
2、随着生物偶联技术的储备增加,针对能够使合成分子有效且位点特异性地附着于蛋白质的化学策略的需求也在增加。在天然蛋白质表面存在大量的诸如赖氨酸和半胱氨酸之类的官能团,这不仅干扰接合的选择性,还会在活性位点导入不优选的接合而导致修饰蛋白质的误操作。此外,现有的生物偶联方式需要诸如遗传修饰或化学处理之类的预处理过程,因此由于在目标的表面无差别地表达而不是在特定位点表达,从而存在无法进行选择性标记的问题。由此,例如以往开发的抗体-药物偶联物(adc)产品以包括低接合抗体、过接合抗体乃至非接合抗体的不均匀的混合物存在的情况较多,并且药物附着位点不具有特异性,因此可能会影响药代动力学、安全性以及疗效特征。由于这种抗体-药物偶联物(adc)的结构的不确定性,存在药物许可失败且会给患者带来无法预测的副作用的问题。
3、因此,需要开发一种用于制备使所需的物质选择性且有效地与多肽的所需的精确位置结合的生物活性偶联物分子的技术。
技术实现思路
1、本发明涉及一种利用包含奥沙宁的适体的偶联物制备。
2、由此,本技术的一具体示例提供一种组合物,其作为包括包含奥沙宁的适体的用于制备多肽的偶联物的组合物,其中,所述适体特异性识别所述多肽。
3、本技术的另一具体示例提供一种包括将所述组合物与多肽混合的步骤的制备多肽的偶联物的方法。
4、本技术的另一具体示例提供一种适体的用途,其作为用于制备多肽的偶联物的包含奥沙宁的适体的用途,其中,所述适体特异性识别所述多肽。
5、本技术的另一具体示例提供一种适体,其作为用于制备多肽的偶联物的包含奥沙宁的适体,其中,所述适体特异性识别所述多肽。
6、本技术的另一示例提供一种包括将包含所述奥沙宁的适体与多肽混合的步骤的制备多肽的偶联物的方法。
7、本技术的另一具体示例提供一种偶联物,其作为包括包含奥沙宁的适体和多肽的偶联物,其中,所述适体特异性识别所述多肽。
8、本技术的另一具体示例提供一种偶联物,其作为包括药物和多肽的偶联物,其中,所述药物通过包含奥沙宁的适体与多肽结合,所述适体特异性识别所述多肽。
9、概览
10、本发明的发明人利用特异性识别多肽的适体的特性以及不使用化学活化过程或反应性接头而与胺基直接反应的奥沙宁的特性,提供一种即使不修饰目标多肽也能够在目标多肽的所需位点以高亲和性和选择性地形成偶联物的技术。具体而言,若在特异性识别目标多肽的适体的序列中引入奥沙宁,则适体可以起到奥沙宁的载体的作用,从而使奥沙宁准确地位于由适体识别的多肽的特定位点,并且在该特定位点处,奥沙宁可以通过与氨基酸(例如,赖氨酸)侧链的胺基反应而形成酰胺键来结合。
11、因此,通过使诸如药物、可检测标记、小分子、聚合体等的第二部分(moiety)与包含奥沙宁的适体结合,使得多肽与第二部分可以借由包含奥沙宁的适体间接缀合(conjugation),因此可以用于制备多种多肽偶联物。作为一实现例,若使药物与含有奥沙宁的适体结合,并用其处理所述适体特异性识别的抗体(多肽),则奥沙宁可以在所述适体特异性识别的抗体的特定位点形成酰胺键,从而形成药物-适体-抗体的偶联物(adc)而用于治疗目的。作为另一实施例,若使荧光团(可检测标记)与含有奥沙宁的适体结合,并用其处理适体特异性识别的抗体(多肽),则奥沙宁在所述适体特异性识别的抗体的特定位点形成酰胺键,从而形成荧光团-适体-抗体的偶联物而用于诊断或检测目的。
12、因此,在本技术中,包含奥沙宁的适体可以在制备多种多肽偶联物(诸如抗体-药物偶联物(adc)之类,但不限于此)时,起到使诸如药物、可检测标记、小分子、聚合体等第二部分与多肽的所需的位置结合的反应剂或交联作用。
13、这种位点特异性偶联物制备的策略基于同时执行1)锁钥(lock-and-key)结合以及2)邻近增强反应(proximity-enhanced reaction)的模块化结构:
14、1)借由适体的锁钥(lock-and-key)结合
15、已知适体是诸如dna和rna之类的核酸,折叠成多种三维结构并以高亲和力和特异性与目标分子结合。适体可以通过被称作典型的试管内进化的体外筛选(in vitroselection)或配体指数富集法系统演化(selex)或其变形的方法来开发。如上所述,若生成能够识别特定目标的适体,则可以起到运输针对目标的反应位点的反应性部分的载体的作用。
16、2)借由奥沙宁的邻近增强反应(proximity-enhanced reaction)
17、已知几种修饰的核碱基随着接近自然界中的丰富的目标官能团(例如,胺、硫醇、羟基等)而显著增加活性。本发明的发明人以序列-特异性方式将作为修饰的核碱基中的一种的奥沙宁(反应性部分)引入适体。如上所述,包含奥沙宁的适体可以以高亲和性和选择性与未损坏的目标的特定位点结合。具体而言,借由适体的基质识别,被引入适体的奥沙宁(反应性部分)可以准确地位于目标的目标位点附近。因此,即使在目标上存在各种官能团,也仅在准确的位置发生耦合。因此,可以适当选择特应性识别目标多肽中包括要缀合的位点在内的位点的适体,从而诱导位点-选择性的缀合。
18、因此,本发明可以提供具有如下特性的新平台:
19、-仅在所需位点以超高特异性和效率形成稳定的化学键;
20、-以没有遗传修饰或化学修饰的天然状态的抗体等天然多肽为目标;
21、-通过产生均匀的偶联物产品而使治疗疗效、安全性以及稳定性最大化;
22、-无需对多肽进行遗传修饰或化学修饰等预修饰,因此工艺简单且方便;
23、-是一种能够普遍应用于多种多肽的通用策略。
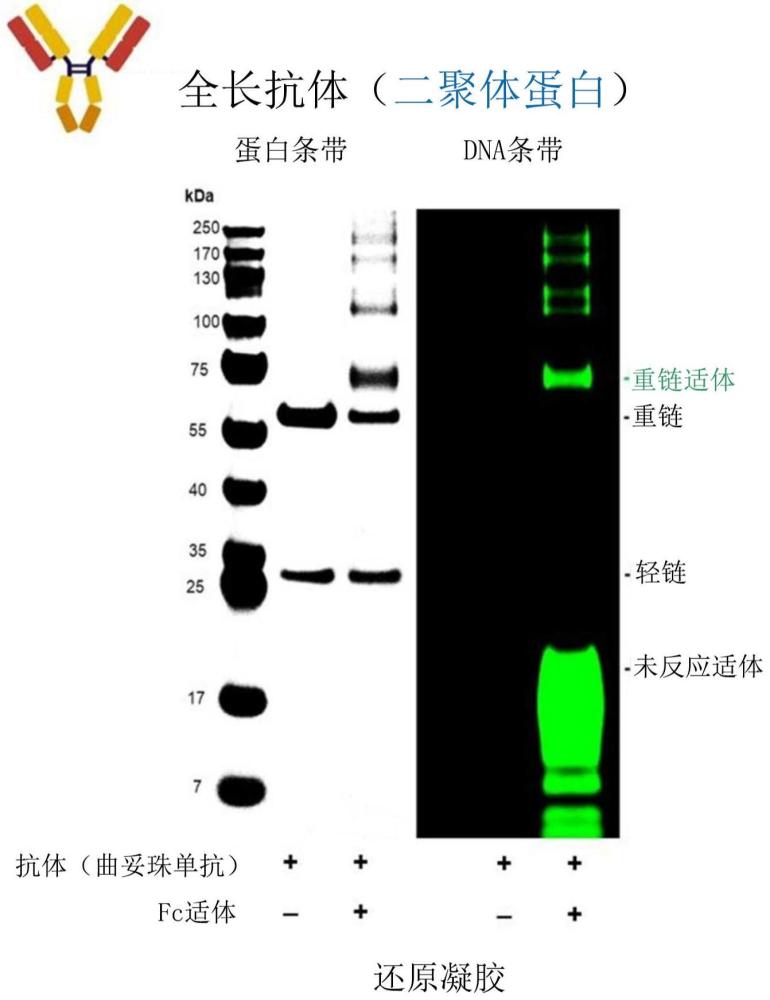
24、实际上,在本技术的一实施例中,以酶(例如,凝血酶)、膜受体蛋白(例如,ptk7)、肿瘤相关核仁蛋白(例如,核仁素)、fc二聚体蛋白以及全长抗体(例如,曲妥珠单抗)等多种多肽为对象确认到,在特异性识别这些多肽的适体引入奥沙宁后,借由与多肽混合的简单的一锅(one-pot)工艺而以较高的超高效率诱导共价结合(图2至图7)。进而,通过在所述抗体-适体偶联物中使药物与适体结合来制备了抗体-适体-药物偶联物(图8),并且确认到所述偶联物在原封不动地保持作为抗体原来所具有的代表性的功能的抗原结合力、fcγr结合力、fcrn结合力等的同时(图9至图11),发挥由药物产生的细胞毒性(图12至图14)。
25、因此,本发明的发明人确认到利用包含奥沙宁的适体是能够通过借由利用适体的钥锁模型的目标识别(target recognition)以及与利用奥沙宁的目标物质的化学反应,来在目标的特定位点以位点-选择性的方式制备偶联物的既简单又强力且可以成为通常的接近方法,从而完成了本发明。
26、根据本发明的一方面,提供一种包括包含奥沙宁的适体的用于制备多肽的偶联物的组合物,其中,所述适体特异性识别所述多肽。
27、本发明的另一方面,提供一种包括将所述组合物与多肽混合的步骤的制备多肽的偶联物的方法。
28、根据本发明的另一方面,提供一种包括包含奥沙宁的适体和多肽的偶联物,其中,所述适体特异性识别所述多肽。
29、根据本发明的另一方面,提供一种包括药物和多肽的偶联物,其中,所述药物通过包含奥沙宁的适体与多肽结合,所述适体特异性识别所述多肽。
30、以下,更加详细地说明本发明。
31、在本说明书(包括权利要求范围)中使用术语“包括(comprise、comprises)”、“含有(comprised)”或“包含(comprising)”的情况下,它们被解释为指定所记载的特征、整数、步骤或构成要素的存在,但是应当解释为不排除存在一个或一个以上的其他特征、整数、步骤、构成要素或它们的组的存在。
32、在本说明书中,关于文献、法令、材料、装置以及物品的说明仅包括用于提供针对本发明的脉络的目的。这些的全部或部分并非提示或表示形成基于现有技术的一部分或在本技术的每项权利要求的优先日之前是本发明所属领域内的通常的一般知识。
33、适体
34、在本技术中,术语“适体(aptamer)”是指其本身具有稳定的三级结构并具有能够与目标分子以高亲和性和特异性结合的特征的单链核酸。在本发明中,适体可以是dna、rna、修饰的核酸或它们的混合物。
35、如上所述,在本技术中,适体特异性识别目标,因此可以起到运输奥沙宁的作用,使得奥沙宁可以准确地位于由适体识别的多肽的特定位点。因此,本技术的适体的特征在于,在其序列中包括作为核碱基之一的奥沙宁。奥沙宁可以被引入到适体的目标识别位点的序列中的任意位点。
36、在本技术中,适体可以是其长度为10至100,或10至90,或10至80,或10至70,或10至60,或10至50,或20至100,或20至90,或20至80,或20至70,或20至60,或20至50,或30至100,或30至90,或30至80,或30至70,或30至60,或30至50,或40至100,或40至90,或40至80,或40至70,或40至60,或40至50个的核苷酸,但不限于此。
37、包含在适体中的各个核苷酸可以各自相同或不同,可以是在核糖(例如,嘧啶核苷酸的核糖)的2'位点上包含羟基的核苷酸(即,未取代的核苷酸),或者可以是在核糖的2'位点上羟基被任意原子或基团所取代的核苷酸。作为这种任意原子或基团,例如,可以是被氢原子、氟原子或-o-烷基(例如,-o-me基)、-o-酰基(例如,-ocho基)、氨基(例如,-nh2基)取代的核苷酸。适体也可以是至少一种(例如,一种、两种、三种或四种)核苷酸在核糖的2'位点上包括选自利用羟基或者上述的任意原子或基团(例如,氢原子、氟原子、羟基以及-o-me基)组成的组中的至少两种(例如,两种、三种或四种)基团的核苷酸。适体也可以是所有核苷酸在核糖的2'位点上包括选自利用羟基或者上述的任意原子或基团(例如,氢原子、氟原子、羟基以及-o-me基)组成的组中的相同的基团的核苷酸。
38、作为一具体示例,在适体中,为了提高针对目标的结合性或稳定性等,各个核苷酸的糖残基(例如,核糖或脱氧核糖)可以被修饰。作为在糖残基上被修饰的位点,例如可以是糖残基的2'位点、3'位点和/或4'位点的氧原子被其他原子取代等。作为修饰的类型,例如可以是氟化、o-烷基化(例如,o-甲基化、o-乙基化)、o-烯丙基化、s-烷基化(例如,s-甲基化、s-乙基化)、s-烯丙基化、氨基化(例如,-nh)。这种糖残基的修饰可以借由自行公知的方法而进行(例如,sproat等人,nucle.acid.res.19,733-738,1991;cotton等人,nucl.acid.res.19,2629-2635,1991;hobbs等人,biochemistry 12,5138-5145,1973)。
39、作为另一具体示例,适体也可以为了提高针对目标的结合性等而使核酸碱基(例如,嘌呤、嘧啶)被修饰(例如,化学取代)。作为这种修饰,例如可以是5位点嘧啶修饰、6和/或8位点嘌呤修饰、环外胺处的修饰、4-硫代尿苷的取代、5-溴或5-碘-尿嘧啶的取代。此外,包含在适体中的磷酸基可以被修饰,以对核酸酶和水解具有耐性。例如,p(0)0基可以被p(0)s(硫代)、p(s)s(二硫代)、p(o)nr2(酰胺)、p(o)r、r(o)or'、co或ch2(甲缩醛)或3'-胺(-nh-ch2-ch2-)取代[其中,每个r或r'独立地为h或者取代或未取代的烷基(例如,甲基、乙基)]。作为连接基团,例示了-o-、-n-或-s-,并且可以通过这些连接基团与相邻的核苷酸结合。修饰还可以包括诸如封端之类的3'和5'的修饰。修饰也可以通过在末端附加聚乙二醇、氨基酸、肽、反向(inverted)dt、核酸、核苷、肉豆蔻酰基(myristoyl)、石胆酸-油烯基(lithocolic-oleyl)、二十二烷基(docosanyl)、月桂酰基(lauroyl)、硬脂酰基(stearoyl)、棕榈酰基(palmitoyl)、油酰基(oleoyl)、亚油酰基(linoleoyl)、除此之外的脂质、类固醇、胆固醇、咖啡因、维生素、色素、荧光物质、抗癌剂、毒素、酶、放射性物质、生物素等来进行。对于这种修饰,可以参照例如美国专利第5,660,985号、美国专利第5,756,703号。
40、在本技术中,适体可以是在本领域公知的特异性识别特定目标的适体,或者可以是为了特异性识别特定目标而制备和筛选的适体。
41、适体可以专门通过称作配体指数富集法系统演化(selex:systematic evolutionof ligands by exponential enrichment)的体外进化方法(in vitro selection)来进行筛选,但不限于此。作为一示例,selex过程首先经过利用dna合成和体外转录(in vitrotranscription)方法(rna的情况)制作具有多种形态的核酸库(>1015),并仅从中筛选能够与所需目标分子结合的核酸结构体的过程。例如,可以通过诸如亲和层析法(affinitychromatography)之类的方法去除(washing)未结合的核酸结构体而只能选择性地获得与目标分子结合的核酸结构体。最后,从目标分子分离(elution)核酸结构体,利用扩增该核酸后获得的核酸结构体再将上述过程重复5~15次左右,从而可以发掘出具有非常优异的结合力和特异性的适体。
42、作为另一示例,还可以执行欲将通过selex获得的适体改良成更稳定且强力的适体的selex后优化(post-selex)过程。作为代表性的示例,用2'-f或2'-nh2、2'-o-甲基取代rna适体的核糖2'-oh。若经过这种变化,则对核酸分解酶的抵抗性优异,从而可以获得在血液内稳定性增加10,000倍以上的适体。
43、除此之外,可以通过本领域已知的多种适体制备方法来获得本技术的适体(例如,参照美国专利5,270,163;5,475,096;5,705,337;5,660,985;5,580,737;6,376,190;7,947,447;7,855,054以及8,409,795;美国专利公开2007016674和20090098549等)。或者,可以采用现有的由本发明的发明人报告的体外进化方法来更有效地获得适体(参照angewchem int ed engl.2016december 05;55(49):15258-15262)。
44、包含奥沙宁的适体
45、奥沙宁(oxanine)作为由鸟嘌呤的亚硝化(nitrosation)生成的环状的核碱基,如图1所示,由于碳二亚胺(carbodiimide)结合的羧基存在于环内,因此可以直接与胺基反应而无需使用化学活化过程或反应性接头。因此,奥沙宁可以通过与氨基酸侧链的胺基(例如,赖氨酸侧链的胺基)反应而形成酰胺键,从而与多肽共价结合。
46、将奥沙宁与核糖(呋喃型)结合的形态称为恶肌苷(oxanosine),并将奥沙宁与脱氧核糖(呋喃型)结合的形态称为脱氧恶肌苷(deoxyoxanosine)。奥沙宁可以通过例如在酸性条件下使脱氧鸟苷与no和/或nano2反应而获得脱氧恶肌苷形态后,对脱氧鸟苷进行酸水解来获得,但不限于此。
47、奥沙宁只要保持被碳二亚胺激活的羧基与胺基的反应性,就可以以任何形态的奥沙宁使用。例如,奥沙宁可以以结合有核糖或脱氧核糖之类的戊糖的形态(即,恶肌苷或脱氧恶肌苷)使用,但不限于此。
48、奥沙宁可以被引入到适体的目标识别位点的序列中的任意位点。奥沙宁被“引入”或“整合”到适体是指奥沙宁被插入到适体的核酸序列中的任意位点。例如,奥沙宁可以被插入到适体的核酸序列中间或末端,并且根据需要,可以在任意位置插入1个或1个以上,例如,2个、3个、4个、5个、6个、7个、8个、9个或10个或10个以上,但不限于此。作为一具体示例,在本技术的实施例中,使用2'-脱氧恶肌苷三磷酸(dotp:2'-deoxyoxanosinetriphosphate)和dna聚合酶建立了在适体内部引入奥沙宁的酶策略。具体而言,奥沙宁是与胞嘧啶形成氢键的鸟苷类似物,因此可以通过使用含有胞嘧啶的dna模板、dna聚合酶以及从5'末端到所需位点的引物的dna链延伸法来将dotp整合于适体链中。第一个延伸步骤在仅包含dotp的反应系统中执行,然后在所需的dntp(n为a、t、c或g)的存在下执行正常的延伸步骤。聚合酶反应后,可以通过去除模板dna来仅获得包含奥沙宁的单链适体。本发明的发明人确认到可以通过这种方法来将dotp插入到dna、rna或修饰的dna/rna杂合链中,这表明该策略可以适用于多种适体。此外,通过适当地设计模板序列,从而可以灵活地指定待插入dotp的位点和数量。通过如上所述的策略可以在适体的核酸序列的任意位点引入奥沙宁,但本发明并不限于此。
49、偶联物
50、术语“偶联物(conjugate)”是指第一部分和第二部分稳定地缔合(stablyassociated)或结合的物质。出于本技术的目的,第一部分和第二部分可以通过包含奥沙宁的适体(反应性部分)缀合。即,第一部分和第二部分可以分别与包含奥沙宁的适体结合(例如,共价结合),因此,第一部分和第二部分可以通过包含奥沙宁的适体间接地缀合。
51、具体而言,第一部分可以是适体特异性识别的多肽。若在特异性识别目标多肽的适体的序列中引入奥沙宁,则适体起到奥沙宁的载体的作用,从而能够使奥沙宁准确地位于由适体识别的多肽的特定位点,并且在该特定位点奥沙宁可以通过与氨基酸(例如,赖氨酸)侧链的胺基反应而形成酰胺键来结合。因此,包含奥沙宁的适体和作为第一部分的多肽可以借由奥沙宁与多肽的共价键而结合。
52、另外,第二部分可以与包含奥沙宁的适体结合。第二部分可以是待与多肽(第一部分)缀合的药物、可检测标记、小分子、聚合体等,但不限于此。
53、第二部分可以与包含奥沙宁的适体的任意位点结合(例如,共价结合)。例如,可以与适体的结构中的目标识别位点以外的位点(例如,不直接参与目标识别并支撑适体的三维结构的位点)结合。本领域技术人员可以根据公知的本领域知识来适当地执行第二部分与适体的结合。例如,适体与第二部分的结合可以是共价结合或非共价结合方式,但不限于此。此外,适体与第二部分的结合可以是直接结合或通过接头的间接结合,但不限于此。此外,适体和第二部分可以是通过与适体互补的寡核苷酸(oligonucleotide)的间接结合,但不限于此。
54、作为一具体示例,由于在适体和第二部分分别有一个以上的官能团,因此可以通过酶合成或化学合成而容易地直接结合。或者,为了直接结合,可以通过在适体和/或第二部分引入官能团来诱导直接结合。作为另一示例,在药物具有在核酸的双链dna结构插入(intercalation)的性质的情况下,可以利用起来结合药物。这种药物可以是具有苯基的疏水性化合物,例如,可以是紫衫烷、喜树(camptotheca)提取物、蒽环类,具体而言,可以是紫杉醇、多西他赛、喜树碱、多柔比星、柔红霉素、表柔红霉素、伊达比星等,但不限于此。
55、作为另一具体示例,适体和第二部分可以通过接头间接地结合。例如,接头可以是可切割接头或不可切割接头。可切割接头可以通过生物环境在体内分离。分离可以由酶、还原、ph等进行,但不限于此。例如,接头在血液的中性ph环境下相对稳定,但在偶联物进入到细胞内部的更低ph环境后可以被切割。作为另一示例,接头在体内酶的作用(例如,蛋白酶的作用)下被切割。酶可分离的基团可以包括以天然核苷酸结束并在其磷酸基末端附着于接头的核苷酸序列。此外,接头可以是肽或非肽接头。接头可以是包括间隔(spacer)部分和两个以上的官能团(functional group)部分的分子,其中,一个官能团用于与适体结合,另一个官能团用于与第二部分结合。官能团作为使适体与第二部分连接的基团,其包括能够结合适体与第二部分的所有官能团。例如,所述官能团可以是胺基(-nh2)、巯基(-sh、sulfhydryl)、-ch、-cooh、烯基、磷酸酯基、硫酸酯基、杂环nh、炔烃基以及酮基等,但不限于此。
56、作为另一具体示例,通过在与适体互补的寡核苷酸结合第二部分并使适体和与其互补的寡核苷酸杂交,其结果,第二部分可以与适体结合(参照实施例6)。
57、因此,作为优选的具体示例,在本技术中,偶联物是多肽偶联物,其中,第一部分作为多肽,且多肽通过包含奥沙宁的适体而与第二部分缀合的多肽偶联物。作为与多肽缀合的第二部分可以例示药物、可检测标记、小分子、聚合体等,但不限于此。第二部分与包含奥沙宁的适体结合,并且奥沙宁在适体特异性识别的多肽的特定位点与侧链包含胺基的氨基酸(例如,赖氨酸)残基形成共价结合,其结果,第二部分可以与多肽的所需的特定位点缀合。
58、此外,多肽可以与1个以上的第二部分(例如,2个、3个、4个、5个、6个、7个、8个、9个、10个或10个以上的第二部分)缀合。作为一例,结合有1个以上的第二部分(例如,2个、3个、4个、5个、6个、7个、8个、9个、10个或10个以上的第二部分)的适体可以与多肽共价结合。作为另一示例,结合有第二部分的适体1个以上(例如,2个、3个、4个、5个、6个、7个、8个、9个、10个或10个以上的适体)可以与多肽共价结合。作为另一示例,1个以上的结合有1个以上第二部分的适体可以与多肽共价结合。
59、多肽
60、术语“多肽”与“肽”和“蛋白质”互换使用,并且是指任意长度的氨基酸的聚合体形态。“多肽”、“肽”以及“蛋白质”包括所有天然产生的多肽或其片段以及合成多肽或其片段。
61、在本技术中,形成偶联物的多肽可以例示治疗性多肽、抗体或其片段、治疗用抗体、诊断用抗体等,但不限于此。以下说明代表性的示例。
62、治疗性多肽
63、治疗性多肽可以以多种目的(例如,血清半衰期的增加、生物活性或生物利用度的增加、免疫原性的增加或减少、副作用的减少等)而形成偶联物。
64、作为治疗性多肽可以例示酶、细胞因子、趋化因子、生长因子、激素、受体、肿瘤相关蛋白等,但不限于此。更具体而言,包括促红细胞生成素(epo)、生长激素、卵泡刺激激素(fsh)、干扰素(例如,ifn-γ、ifn-α、ifn-β、ifn-ω、ifn-τ、共有干扰素等)、胰岛素、胰岛素样生长因子(例如,igf-i、igf-ii等)、血液因子(例如,因子x、组织纤溶酶原激活因子(tpa)、因子viia、因子viii、因子ix、β-珠蛋白、血红蛋白等)、菌落刺激因子(例如,粒细胞-csf(g-csf)、巨噬细胞-csf(m-csf)、粒细胞-巨噬细胞-csf(gm-csf)、粒细胞-单胞菌落刺激因子、巨核细胞单胞菌落刺激因子等)、转化生长因子(例如,tgf-β、tgf-α)、白细胞介素(例如,il-1、il-2、il-3、il-4、il-5、il-6、il-7、il-8、il-9、il-12等)、血小板衍生因子(pdgf)、成纤维细胞生长因子(fgf,例如,afgf、bfgf)、胶质细胞株来源生长因子(gdnf)、神经生长因子(ngf)、干细胞因子、角蛋白细胞生长因子、肝细胞生长因子等)、可溶性受体(例如,tnf-α-结合可溶性受体、可溶性vegf受体、可溶性白细胞介素受体、可溶性γ/δt细胞受体等)、酶(例如,凝血酶、α-葡萄糖苷酶、β-葡糖脑苷脂酶等)、趋化因子(例如,ip-10、mig、groα/il-8、rantes、mip-1α、mip-1β、mcp-1、pf-4等)、血管新生剂(例如,血管内皮生长因子(vegf))、抗血管新生剂(例如,可溶性vegf受体)、蛋白疫苗、神经刺激肽、血栓溶解剂、心房钠尿肽、骨形成蛋白质、血小板生成素、松弛素、神经胶质纤维酸性蛋白、肿瘤坏死因子、中性粒细胞趋化因子、血管紧张素、血管营养素、纤维蛋白、水蛭素等,但不限于此。
65、抗体或其片段
66、在本技术中,术语“抗体”是指与特定抗原或抗原决定簇特异性结合的蛋白质的总称,以最广泛的含义使用,并且可以是在免疫系统内经抗原的刺激而产生的蛋白质或对其进行化学合成或重组而制备的蛋白质,其类型不受特别的限制。具体而言,包括单克隆抗体(包括全长单克隆抗体)、多克隆抗体、多特异性抗体(例如,双特异性抗体)、合成抗体(或也称为抗体模拟物)、嵌合抗体、人源化抗体、人源抗体或抗体融合蛋白(或也称为抗体偶联物),只要表现出所需的生物活性即可。此外,抗体可以是治疗用抗体或诊断用抗体,但不限于此。
67、术语“单克隆抗体”是指从实质上相同的抗体群中获得的单分子组成的抗体分子,对特定抗原决定簇表现出单一结合特异性和亲和性。术语“多克隆抗体”是指包含与相同抗原的不同抗原决定簇结合的两个以上的单克隆抗体的抗体混合物,并且可以与多个抗原决定簇反应。术语“嵌合抗体”是重组非人源抗体的可变区和人源抗体的恒定区的抗体,其是与非人源抗体相比显著改善免疫反应的抗体。术语“人源化抗体”是指将非人源抗体的cdr序列的全部或部分移植到人源抗体的形态的抗体,作为其示例,可以通过将小鼠单克隆抗体的cdrs与人源抗体来源的骨架区(fr:framework region)重组而制备人源化可变区,并使其与优选的人源抗体的恒定区重组来制备,但不限于此。术语“人源抗体”是指完全没有非人类动物来源部分的抗体。通常,人源抗体是指包括cdr区和fr区的可变区和恒定区均来源于人生殖系免疫球蛋白序列的抗体。
68、完整抗体(例如,igg型)是具有两个全长(full length)轻链和两个全长重链的结构,并且是分别由一条重链拷贝和一条轻链拷贝构成的异源二聚体(heterodimer)以y字形排列的同源二聚体(homodimer)。每条轻链通过二硫化键与重链连接。抗体的恒定区分为重链恒定区和轻链恒定区,重链恒定区具有伽马(γ)、缪(μ)、阿尔法(α)、德尔塔(δ)或伊普西龙(ε)类型,并且具有伽马1(γ1)、伽马2(γ2)、伽马3(γ3)、伽马4(γ4)、阿尔法1(α1)或阿尔法2(α2)作为亚类。轻链的恒定区具有卡帕(κ)和拉姆达(λ)类型。
69、术语“重链(heavy chain)”被解释为将包括包含具有足以用于对抗原赋予特异性的可变区序列的氨基酸序列的可变区结构域vh以及三个恒定区结构域ch1、ch2、ch3以及铰链(hinge)的全长重链及其片段两者全部包括的含义。
70、术语“轻链(light chain)”被解释为将包括包含具有足以用于对抗原赋予特异性的可变区序列的氨基酸序列的可变区结构域vl以及恒定区结构域cl的全长轻链及其片段两者全部包括的含义。
71、术语“互补性决定区(cdr:complementarity-determining regions)”是指在抗体的可变区中赋予与抗原的结合特异性或结合亲和性的位点。通常,在重链可变区中存在三个cdr(cdr-h1、cdr-h2、cdr-h3),在轻链可变区中存在三个cdr(cdr-l1、cdr-l2、cdr-l3)。所述cdr可以在抗体或其片段与抗原或抗原决定簇结合时提供主要的接触残基。“骨架区(fr:framework region)”是指重链和轻链的可变区的非cdr部分,通常,在重链可变区中存在四个fr(fr-h1、fr-h2、fr-h3以及fr-h4),在轻链可变区中存在四个fr(fr-l1、fr-l2、fr-l3以及fr-l4)。给定的cdr或fr的精确氨基酸序列边界可以通过使用多种众所周知的体系(卡巴特(kabat)编号系统、科蒂亚(chothia)编号系统、接点(contact)编号系统、imgt编号系统、aho编号系统、abm编号系统等)中的一种来容易地确定。
72、术语“可变区(variable region)”是指参与使抗体与抗原结合的抗体重链或轻链的结构域。重链可变(vh)区和轻链可变(vl)区通常具有相似的结构,每个结构域包括四个保守骨架区(fr)和三个cdr。
73、术语“抗体的片段”是指存在于抗体的全长链的氨基酸中的至少一部分缺失的抗体的任意片段。抗体的片段可以包括例如fc、f(ab')2、单链可变片段(scfv:single chainvariable fragment)(例如,scfv、(scfv)2等)、抗原结合片段(fab:fragment antigenbinding)(例如,fab、fab'、f(ab')2等)、结构域抗体、肽体、小体、内体、二体、三体、四体以及单链抗体等,但不限于此。此外,抗体的片段可以是scfv,或者可以是scfv与免疫球蛋白(例如,iga、igd、ige、igg(igg1、igg2、igg3、igg4)、igm等)的fc位点融合的融合多肽(scfv-fc)或与轻链的恒定区(例如,卡帕或拉姆达)融合的融合多肽(scfv-cκ(卡帕恒定区)或scfv-cλ(拉姆达恒定区)),但不限于此。
74、治疗用抗体
75、术语“治疗用抗体”是指在治疗疾病时使用的抗体。治疗用抗体可以具有多种作用机制。治疗用抗体可以与目标结合并中和其正常的功能。例如,阻断癌细胞的生存所需的蛋白质的活性的单克隆抗体会导致癌细胞的死亡。另一种治疗用单克隆抗体可以与目标结合并激活其正常的功能。例如,单克隆抗体可以与细胞上的蛋白质结合而触发细胞凋亡信号。最后,在单克隆抗体与仅在患有疾病的组织表达的目标结合的情况下,使毒性有效载荷(payload)(有效作用剂)(例如,化学疗法剂或放射能作用剂)与单克隆抗体接合,并向患有疾病的组织特异性传递毒性有效载荷,从而可以生成减少对健康组织的危害的作用剂。
76、治疗用抗体可以是为了治疗多种疾病(例如,癌(例如,血癌和实体癌)、免疫疾病、神经系统疾病、血管疾病或感染性疾病等)而使用的抗体。针对这种抗体的抗原可以是源自肿瘤抗原(例如,肿瘤相关抗原(taa:tumor-associated antigen)、肿瘤-特异性抗原(tsa:tumor-specific antigen)或肿瘤来源新生抗原(neoantigen))、感染源的抗原(例如,源自病毒、细菌、寄生虫或真菌)、已知或疑似诱发自身免疫的自体抗原或者已知或疑似诱发过敏的过敏诱发抗原(过敏原)的肽,但不限于此。
77、例如,这种抗体可以是alk、附着相关激酶受体(例如,axl),或erbb受体(例如,egfr、erbb2、erbb3、erbb4),或产生促红细胞生成素的肝细胞(eph)受体(例如,epha1、epha2、epha3、epha4、epha5、epha6、epha7、epha8、ephb1、ephb2、ephb3、ephb4、ephb5、ephb6),或成纤维细胞生长因子(fgf)受体(例如,fgfr1、fgfr2、fgfr3、fgfr4、fgfr5),或fgr或igf1r或胰岛素受体,或ltk,或m-csfr,或musk,或血小板诱导生长因子(pdgf)受体(例如,pdgfr-a、pdgfr-b),或ret,或ror1,或ror2,或ros,或ryk,或血管内皮生长因子(vegf)受体(例如,vegfr1/flt1、vegfr2/flk1、vegf3),或具有免疫球蛋白样及egf样区的酪氨酸激酶(tie)受体(例如,tie-1、tie-2/tek),或tec,或tyro10,或胰岛素样生长因子(igf)受体(例如,ins-r、igf-ir、ir-r),或盘状结构域(dd:discoidin domain)受体(例如,ddr1、ddr2),或针对c-met(met)的受体,或受体酪氨酸激酶(recepteur d'originenantais)(ron,已知也称为巨噬细胞刺激1受体),或flt3(鳍(fins)相关酪氨酸激酶3),或菌落刺激因子1(csf 1)受体,或针对c-kit的受体(kit或scfr),或胰岛素受体相关(irr)受体,或cd19,或cd20,或hla-dr,或cd33,或cd52,或g250,或gd3,或psma,或cd56,或cea,或路易斯(lewis)y抗原,或针对il-6受体的抗体,但不限于此。
78、诊断用抗体
79、术语“诊断用抗体”是指用作诊断疾病的试剂的抗体。诊断用抗体可以与特定疾病特异性相关,或者与在特定疾病中表示增加的表达的目标生物标志结合。诊断用抗体可以用于例如来自患者的生物样本中的目标检测或患者内疾病位点(例如,肿瘤)的诊断成像。
80、诊断用抗体可以与一个以上的可检测标记结合,以易于实现所结合的抗原的检测和/或定量。这种标记可以包括荧光物质、生物素部分和/或酶,但不限于此。例如,酶可以包括诸如辣根过氧化物酶(hrp)之类的过氧化物酶(peroxidase)、碱性磷酸酶(alkalinephosphatase)等,荧光物质可以包括fitc、ritc等,此外可以使用放射性同位素标记、乳胶珠标记、胶体标记、生物素标记等,但不限于此。
81、多肽偶联物
82、如上所述,作为诸如治疗性多肽、抗体或其片段之类的与多肽缀合的部分(第二部分),可以例示药物、可检测标记、小分子、聚合体等,但不限于此。这些也可以被称为“有效载荷(payload)”或“货物(cargo)”,但不限于此。
83、药物包括多肽、化合物、小分子、提取物、核酸等,但不限于此。
84、小分子是指表现出药物活性的通常分子量为约800da以下或2000da以下的化合物,但不限于此。无机小分子是指不含有碳原子的分子,有机小分子是指含有至少一个碳原子的化合物。
85、可检测的标记的具体示例包括荧光分子(例如,自发荧光分子、与试剂接触时发出荧光的分子等)、放射性标记(例如,111in、125i、131i、212b、90y、186rh等),生物素(例如,通过生物素和亲和素的反应来检测)、荧光标记、造影试剂等,但并不限于这些。可检测标记还包括能够借由抗体结合(例如,可检测地标记的抗体的结合或经由夹心型检查的结合的抗体的检测)而检测出的肽或多肽。可检测标记的追加的示例包括染料标记(例如,发色团、荧光团,例如但不限于alexa fluor(注册商标)荧光染料(例如,alexa fluor(注册商标)350、405、430、488、532、546、555、568、594、595、610、633、635、647、660、680、700、750、790等)、生物理学探针(自旋标记(spin label)、核磁共振(nmr)探针)、荧光共振能量转移(fret)型标记(例如,包括荧光团/猝灭(quencher)对的至少一个成员的fret对中的至少一个成员)、生物发光共振能量转移(bret)型标记(例如,bret对中的至少一个成员)、可免疫检测标记(例如,flag、his(6)等)、局部标记等,但不限于这些。
86、聚合体包括例如水溶性聚合体,但不限于此。例如,聚乙二醇(peg)可以与多肽进行缀合而增加多肽的血清半衰期或降低免疫原性。除此之外,包括葡聚糖及葡聚糖衍生物(例如,葡聚糖硫酸酯、p-氨基交联糊精以及羟甲基糊精)、纤维素及纤维素衍生物(例如,甲基纤维素及羧甲基纤维素、淀粉及糊精以及淀粉的衍生物及羟乳酸酯(hydroylactes)),聚亚烷基二醇及其衍生物(例如,甲氧基聚乙二醇、聚乙二醇同种聚合体、聚丙二醇同种聚合体、乙二醇和丙二醇的共聚物),所述同种聚合物和共聚物可以在一个末端由烷基、肝素及肝素的片段、聚乙烯醇及聚乙烯醚、聚乙烯吡咯烷酮、天冬酰胺及聚氧乙基化多元醇、葡聚糖及葡聚糖衍生物、糊精及糊精衍生物被取代或未被取代。
87、出于本技术的目的,与多肽缀合的部分(第二部分)可以与包含奥沙宁的适体结合(例如,共价结合),因此,多肽和第二部分可以通过包含奥沙宁的适体间接地缀合。
88、在本技术中,作为多肽偶联物的代表性的实现例,将在以下说明抗体-药物偶联物(adc:antibody-drug conjugate)和fc片段-药物偶联物。
89、抗体-药物偶联物(adc:antibody-drug conjugate)
90、术语“抗体-药物偶联物(adc:antibody-drug conjugate)”使抗体与治疗活性物质或活性药物成分(api)缀合,从而使药物对抗体靶向的结合目标发挥药理性的功能。治疗活性物质或活性药物成分可以是能够杀死恶性细胞或癌细胞的细胞毒素,或者可以是诸如抗生剂、核酸分解酶之类的酶以及放射线核素等,但不限于此。出于本技术的目的,治疗活性物质或活性药物成分与包含奥沙宁的适体结合(例如,共价结合),并且在适体特异性识别的抗体的特定位点上,奥沙宁与抗体的赖氨酸残基形成共价结合,其结果,治疗活性物质或活性药物成分可以与抗体的所需的特定位点缀合。
91、术语“细胞毒素”和“细胞毒性剂”是指表现出抑制或阻止细胞的功能和/或引起细胞的破坏(细胞死亡)和/或抗增殖效果的任意分子。应理解adc的细胞毒素或细胞毒性剂在本领域中也被称为adc的“有效载荷(payload)”。在本领域已知细胞毒性剂的很多类别在adc分子中具有潜在的效用,并且可以在本技术中公开的adc中被使用。这些细胞毒性剂的类别包括微管蛋白(microtubulin)结构形成抑制剂、有丝分裂(mitosis)抑制剂、拓扑异构酶(topoisomerase)抑制剂或dna嵌入剂(dna intercalators),但不限于此。具体的细胞毒性剂的具体示例包括美登素衍生物(maytansinoid)、奥瑞他汀(auristatin)、多拉司他汀(dolastatin)、单端孢霉烯(trichothecene)、cc-1065药物(nsc 298223)、卡奇霉素(calicheamicin)、烯二炔类(enediynes)、紫衫烷(taxane)、蒽环霉素(anthracycline)、甲胺喋呤(methotrexate)、阿霉素(adriamycin)、硫酸长春地辛(vindesine)、长春花生物碱(vinca alkaloid)、多柔比星(doxorubicin)、美法仑(melphalan)、丝裂霉素c(mitomycinc)、苯丁酸氮芥(chlorambucil)、柔红霉素(daunorubicin)、道诺霉素(daunomycin)、依托泊苷(etoposide)、替尼泊甙(teniposide)、卡柔比星(carminomycin)、氨基蝶呤(aminopterin)、更生霉素(dactinomycin)、博来霉素(bleomycin)、埃斯培拉霉素(esperamicin)、5-氟尿嘧啶(5-fluorouracil)、、氮芥(盐酸氮芥)[nitrogen mustar(mechlorethamine hcl)]、顺铂及其同系物、顺氯氨铂(cisplatin)、cpt-11、、多西他赛(docetaxel),但不限于此。
92、fc片段-药物偶联物
93、与fc片段形成偶联物的“药物”是指在对人类或动物给药的情况下表现出治疗活性的物质,包括多肽、化合物、小分子、提取物、核酸等,但不限于此。作为多肽药物包括激素类(肠激素、生长激素释放激素、生长激素释放肽等)、干扰素类(干扰素-α、-β、-γ等)、白细胞介素类、生长因子类、粒细胞菌落刺激因子(g-csf)、粒细胞-巨噬菌落刺激因子(gm-csf)、胰高血糖素样肽类(glp-1等)、红细胞生成因子、酶等,但不限于此。此外,只要具有与所述多肽药物的天然型实质上等同或增加的功能、结构、活性或稳定性,任何衍生物都将包括在本发明的多肽药物的范围内。
94、除了多肽药物以外,多种药物可以与fc片段连接,可以例示有:选自四环素、米诺环素、强力霉素、氧氟沙星、左氧氟沙星、环丙沙星、克拉霉素、红霉素、头孢克洛、头孢噻肟、亚胺培南、青霉素、庆大霉素、链霉素、万古霉素等的衍生物及混合物中的抗生剂;选自甲胺喋呤、卡铂、泰素、顺氯氨铂、5-氟尿嘧啶、多柔比星、依托泊苷、紫杉醇、喜树碱、阿糖胞苷等的衍生物及混合物中的抗癌剂;选自吲哚美辛、布洛芬、酮洛芬、匹洛西卡、氟比洛芬、双氯芬酸等的衍生物及混合物的消炎剂;选自阿昔洛韦、利巴韦林等的衍生物及混合物中的抗病毒剂;以及选自酮康唑、伊曲康唑、氟康唑、两性霉素b、灰黄霉素等的衍生物及混合物中的抗菌剂;等,但并不限于此。
95、通常,抗体的fc区是由重链ch2和ch3结构域构成的重链片段的二聚体形态,根据情况还会包括铰链(hinge)部分。本发明的fc片段可以是仅排除免疫球蛋白的重链和轻链可变区而包括部分或整个重链恒定区1(ch1)和/或轻链恒定区1(cl1)的扩展的fc区,只要具有与天然型实质上等同或提高的效果即可。此外,也可以是去除对应于ch2和/或ch3的氨基酸序列中的一部分的区。此外,在本发明中,fc片段不仅包括天然型氨基酸序列,还包括其的序列衍生物(mutant)。氨基酸序列衍生物是指因天然氨基酸序列中的一个以上的氨基酸残基缺失、插入、非保守或保守取代或它们的组合而具有不同的序列。此外,在本发明中,fc片段可以是天然型糖链、相比天然型增加糖链、相比天然型减少糖链或糖链被去除的形态。
96、此外,fc片段可以是同源二聚体(homodimer)或异源二聚体(heterodimer)。通常,fc片段的同源二聚体化由抗体恒定区的最后一个结构域(在igg的情况下,ch3结构域)之间的非共价键以及铰链区之间的二硫键被诱导。fc片段的异源二聚体可以通过以借由对自然产生的抗体同型二聚体化做贡献的恒定区的最后一个结构域之间的特定非共价结合而具有偏好异二聚体化且不偏好或排斥同型二聚体化的结合的方式进行设计来制备。例如,可以通过基因操作在各自不同的两条ig抗体重链的ch3结构域诱导突变,从而可以诱导两条重链的结构与自然产生的抗体非常相似且在序列上具有最小的偏差而形成异源二聚体。作为与此相关的技术,可以例示美国基因泰克(genentech)公司的旋钮插入孔(knob-into-hole)技术、zymeworks公司的zw1、xenecore公司的ha-tf、emd serono公司的seedbody等,但不限于此。
97、剂型、组合物以及方法
98、在本技术中,偶联物可以以多种方式配制。通常,在偶联物是多肽-药物偶联物的情况下,偶联物可以以与多肽缀合的药物、待治疗的病情以及所利用的给药途径相容的方式配制。偶联物(例如,多肽-药物偶联物)可以以任何合适的形态(例如,药剂学上可允许的盐的形态)被提供,并且可以配制成用于任何合适的给药途径(例如,口服、局部或肠胃外给药途径)。在偶联物作为液体可注射物质(例如,它们直接给药到静脉内或组织内的实施方式)被提供的情况下,偶联物可以以可即用的(ready-to-use)给药形态,或药剂学上可允许的载体或由赋形剂组成的可重组的储存稳定性粉末或液体被提供。
99、配制偶联物的方法可以从本领域中可使用的方法中适用。例如,偶联物可以以包含治疗有效量的偶联物以及药剂学上可允许的载体(例如,盐水)的药剂学组合物被提供。药剂学组合物可以选择性地包含其他添加物(例如,缓冲剂、稳定剂、保存剂等)。在一些实施方式中,剂型是适合于向哺乳动物给药的剂型,尤其是,适合于向人类给药的剂型。
100、在本技术的偶联物用作治疗用途的情况下,包含偶联物的组合物的给药可以预防疾病,或者可以阻碍、终止或延迟疾病状态的发病或进展,或者可以使症状好转或改善。
101、因此,本技术还提供一种包含有效量的本技术的偶联物的治疗用组合物及将其向个体给药的步骤的治疗方法。
102、术语“有效量”是指向包括人类在内的个体给药时足以实现所需的结果的量(例如,有效治疗或预防疾病的量)。有效量可以根据诸如制剂方法、给药方式、患者的年龄、体重、性别、疾病的严重程度、饮食、给药时间、给药途径、排泄速度以及反应敏感性之类的多种因子而不同。给药量或治疗方案可以调整为本领域技术人员所理解的提供最佳的治疗反应。
103、本技术的组合物可以与选自利用药学上可允许的载体、稀释剂以及赋形剂等组成的组中的一种以上的添加剂一起提供。
104、所述药学上可允许的载体作为通常用于制剂的载体,例如,可以是选自利用乳糖、右旋糖、蔗糖、山梨糖醇、甘露醇、淀粉、阿拉伯胶、磷酸钙、藻酸盐、明胶、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮、纤维素、水、糖浆、甲基纤维素、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石、硬脂酸镁,矿物油等组成的组中的一种以上,但不限于此。除了上述成分以外,组合物还可以包含选自利用在药学组合物制备中通常使用的稀释剂、赋形剂、润滑剂、润湿剂、甜味剂、调味剂、乳化剂、悬浮剂、保存剂等组成的组中的一种以上。包括上述的示例在内的适合于本发明的药学上可允许的载体及制剂在文献[雷明顿制药科学(remington'spharmaceutical sciences),最新版]中被详细记载。
105、组合物可以口服或肠外给药。在肠外给药的情况下,可以通过静脉内注射、皮下注射、肌肉注射、腹腔注射、内皮给药、局部给药、鼻内给药、眼内给药、脊柱内给药、脑膜内给药、颅内给药、纹状体内给药等进行给药。
106、在部分实现例中,组合物可以作为无菌液体制剂提供,例如,可以以等渗水溶液、悬浮液、乳液、分散液或粘性组合物被提供,其在一些方面可以缓冲为所选的ph。液体制剂通常比凝胶剂、其他粘性组合物以及固体组合物更加容易制备。此外,液体组合物尤其便于通过注射方式给药。另一方面,粘性组合物可以在合适的粘度范围内配制,以提供与特定组织的更长的接触时间。液体或粘性组合物可以包含载体,其可以是含有例如水、盐水、磷酸盐缓冲盐水、多元醇(例如甘油、丙二醇、液体聚乙二醇)及其合适的混合物的溶剂或分散介质。
107、无菌注射用溶液可以通过将结合分子整合到合适的载体、稀释剂或与诸如无菌水、生理盐水、葡萄糖、右旋糖等赋形剂的混合剂之类的溶剂来制备。组合物也可以被冷冻干燥。组合物可以根据给药途径及所需的制备途径而含有诸如润湿剂、分散剂或乳化剂(例如,甲基纤维素)、ph缓冲剂、凝胶化或粘度增强添加剂、防腐剂、调味剂、色素等辅助物质。
108、可以添加包括抗菌防腐剂、抗氧化剂、螯合剂以及缓冲液的提高组合物的稳定性和杀菌性的多种添加剂。微生物的作用的预防可以通过多种抗菌及抗真菌剂(例如,对羟苯甲酸、氯丁醇、苯酚、山梨酸等)来保证。注射用药学形态的长时间吸收可能是由延迟吸收的制剂(例如,单硬脂酸铝以及明胶)的使用而导致的。
本文地址:https://www.jishuxx.com/zhuanli/20241021/320124.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表