一种工程化克劳氏芽孢杆菌胞外囊泡、药物递送载体及其制备方法和应用
- 国知局
- 2024-11-06 15:03:51
本发明属于生物医药,具体涉及一种工程化克劳氏芽孢杆菌胞外囊泡、药物递送载体及其制备方法和应用。
背景技术:
1、恶性肿瘤起病隐匿、进展迅速、预后极差,极大地影响患者生存期,多数患者在就诊时即为晚期,失去根治性手术机会。恶性肿瘤化疗的综合治疗模式中,维持治疗占有重要地位,病情经治疗后得到一定控制,需要进一步维持治疗,将稳定的状态得以“维持”,可延缓复发时间,从而延长患者无进展生存期(pfs)。因此,维持治疗可看作是化疗后延长肿瘤患者生存期的最主要途径。
2、olaparib(奥拉帕尼,ola)是第一个被批准用于肿瘤类型的parpi,目前在临床上用于铂敏感的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌、brca突变晚期卵巢癌、携带brca突变的晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌、胰腺癌、前列腺癌等恶性肿瘤的维持治疗。与安慰剂相比,ola改善pfs具有统计学意义,给恶性肿瘤患者带来极大希望。然而,ola适应症有限,目前仅对携带brca突变且一线含铂基础化疗达到稳定的恶性肿瘤患者有效,而这部分患者临床占比不足10%。因此,针对非brca基因突变者,需加强双链修复的抑制。
3、rad51是一种dna重组酶,在同源重组过程中促进同源配对和链交换,对双链修复起关键作用,已被证明在胰腺癌、甲状腺癌、肾透明细胞癌、子宫内膜样腺癌、前列腺癌、头颈部鳞状细胞癌等恶性肿瘤中过表达,因此高效阻断rad51表达,有望强力抑制双链修复。sirna介导的rna干扰是在进化中高度保守的、由sirna诱发的、同源mrna高效特异性降解现象,具有选择性强、特异性好、作用迅速、基因沉默效率高等特点,成为肿瘤治疗的热门工具。采用sirna介导的rna干扰策略用于rad51沉默,可模拟brca基因突变,联合ola起到“合成致死”作用,对非brca突变患者受益显著,大大拓宽ola的适应症。
4、此外,ola存在一定不良反应,给药后体内分布无选择性,导致血液学及消化系统毒性,需加强药物靶向递送与浓集以减少不良反应。细菌胞外囊泡(bevs)是由革兰阴性/阳性菌自发形成、直径10-400nm的球形双层纳米结构。bevs的一个重要作用是为其亲本细胞将生物分子运送至特定的远端位置,基于该现象,学者们提出胞外囊泡可成为一种新型药物载体的假设。肠道益生菌——克劳氏芽孢杆菌(b.clausii)能够形成内孢子,这种内孢子能够抵抗环境压力源,如热、酸性胃液ph值和胆汁,这些特性使芽孢杆菌益生菌能够在恶劣的消化道条件下更好地存活,并以完整的形式到达肠道,发挥健康益处。bevs具有与亲本细菌相似的生物学功能,如果选择肠道益生菌b.clausii胞外囊泡作为药物递送载体,具有胃肠道及体液循环稳定性,可同时用于口服或注射给药,更重要的是,与致病菌来源bevs相比,b.clausii胞外囊泡不含毒力因子,无潜在安全风险。
5、半乳凝素(gal)家族是一类能识别糖蛋白和糖脂的特异性低聚糖可溶性凝集素,galectin-3(也称lgals3)是gal家族中一员,在胰腺癌、甲状腺癌、肾透明细胞癌、子宫内膜样腺癌、前列腺癌、头颈部鳞状细胞癌等恶性肿瘤中高表达。g3-c12(氨基酸序列为antpcgpythdcpvkr)是高度亲和galectin-3受体的多肽,其所修饰的纳米药物可通过高度特异性的配体-受体方式主动靶向并内化到galectin-3过表达的肿瘤细胞中。如果肠道克劳氏芽孢杆菌bevs,膜表面通过基因工程技术表达与galectin-3特异性结合的g3-c12,可加强对胰腺癌、甲状腺癌、肾透明细胞癌、子宫内膜样腺癌、前列腺癌、头颈部鳞状细胞癌等恶性肿瘤的选择性,赋予bevs靶向能力,同时对转移性恶性肿瘤也可产生主动靶向效应,由此对于原发瘤及转移瘤均具有靶向浓集功能。
技术实现思路
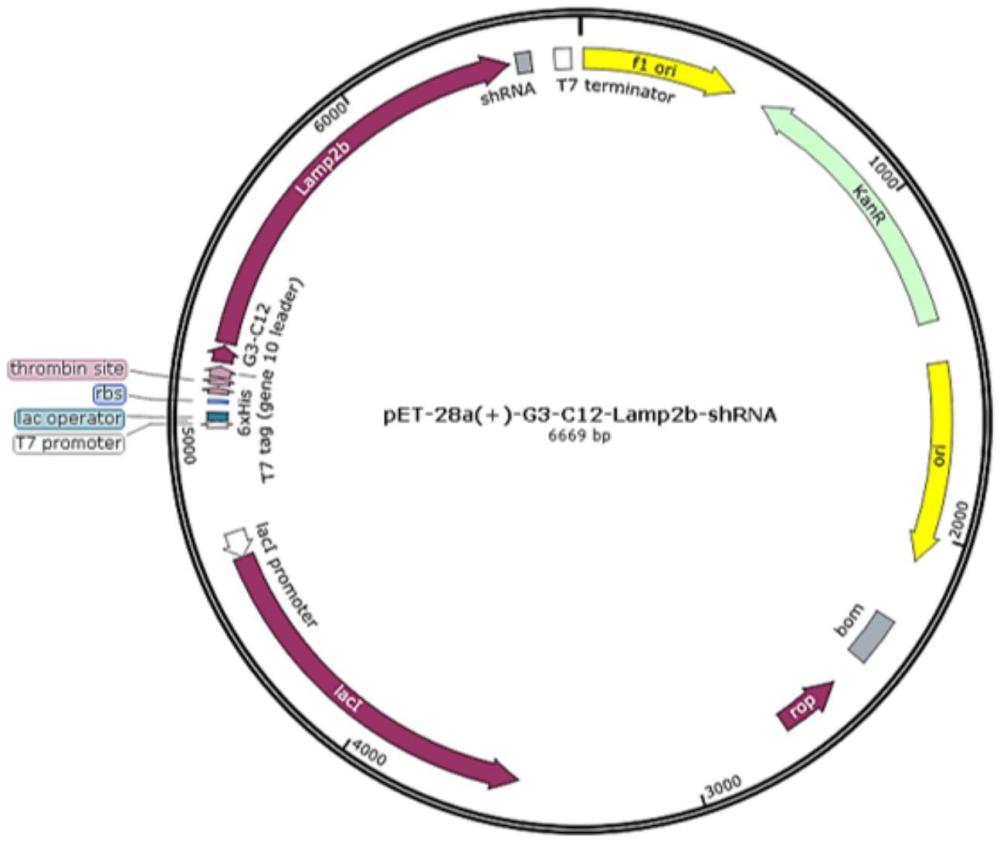
1、基于此,本发明的主要目的在于提供一种工程化克劳氏芽孢杆菌胞外囊泡,通过基因工程设计重组质粒pet-28(+)-g3-c12-lamp2b-shrna,转化入b.clausii后实现共表达,获取携带rad51 sirna且表面表达g3-c12的工程化囊泡(ebevs)。
2、本发明的另一目的在于提供一种药物递送载体,其包括所述工程化克劳氏芽孢杆菌胞外囊泡,将ola负载于ebevs,构建一种药物递送系统ebevs-ola,给药方式灵活,可通过口服或注射给药。
3、本发明的再一目的在于提供所述工程化克劳氏芽孢杆菌胞外囊泡或所述药物递送载体在制备治疗癌症的药物中的应用,利用g3-c12主动靶向并浓集于原发瘤及转移瘤,且通过膜融合实现ola和rad51 sirna的胞内释放,rad51 sirna特异性沉默rad51,ola同步作用于parp酶,联合抑制dna损伤修复,产生“合成致死”作用,显著提升基于ola的维持疗法在治疗胰腺癌、甲状腺癌、肾透明细胞癌、子宫内膜样腺癌、前列腺癌、头颈部鳞状细胞癌等恶性肿瘤中的应用和疗效,从而有效延长患者生存期。
4、为实现上述目的,本发明提供如下技术方案:
5、本发明提供一种工程化克劳氏芽孢杆菌胞外囊泡,其携带rad51 sirna且表面表达g3-c12,先通过基因工程设计构建pet-28(+)-g3-c12-lamp2b-shrna重组质粒,再转化入克劳氏芽孢杆菌(b.clausii)后实现共表达而得。
6、本发明还提供所述工程化克劳氏芽孢杆菌胞外囊泡的制备方法,包括以下步骤:
7、(1)基因工程设计构建pet-28(+)-g3-c12-lamp2b-shrna重组质粒,包括:
8、(a)人工合成如seq id no:1所示的g3-c12多肽的dna编码序列,与lamp2b cdna融合,得到如seq id no:2所示的g3-c12-lamp2b融合基因序列;具体地,所述g3-c12多肽的dna编码序列为gccaacacaccatgtggcccctacacccacgactgccctgtgaagaga(seq id no:1);所述g3-c12-lamp2b融合基因序列为:gccaacacaccatgtggcccctacacccacgactgccctgtgaagagaggcagtggagtgtgcttccgcctcttcccggttccgggctcagggctcgttctggtctgcctagtcctgggagctgtgcggtcttatgcattggaacttaatttgacagattcagaaaatgccacttgcctttatgcaaaatggcagatgaatttcacagtacgctatgaaactacaaataaaacttataaaactgtaaccatttcagaccatggcactgtgacatataatggaagcatttgtggggatgatcagaatggtcccaaaatagcagtgcagttcggacctggcttttcctggattgcgaattttaccaaggcagcatctacttattcaattgacagcgtctcattttcctacaacactggtgataacacaacatttcctgatgctgaagataaaggaattcttactgttgatgaacttttggccatcagaattccattgaatgacctttttagatgcaatagtttatcaactttggaaaagaatgatgttgtccaacactactgggatgttcttgtacaagcttttgtccaaaatggcacagtgagcacaaatgagttcctgtgtgataaagacaaaacttcaacagtggcacccaccatacacaccactgtgccatctcctactacaacacctactccaaaggaaaaaccagaagctggaacctattcagttaataatggcaatgatacttgtctgctggctaccatggggctgcagctgaacatcactcaggataaggttgcttcagttattaacatcaaccccaatacaactcactccacaggcagctgccgttctcacactgctctacttagactcaatagcagcaccattaagtatctagactttgtctttgctgtgaaaaatgaaaaccgattttatctgaaggaagtgaacatcagcatgtatttggttaatggctccgttttcagcattgcaaataacaatctcagctactgggatgcccccctgggaagttcttatatgtgcaacaaagagcagactgtttcagtgtctggagcatttcagataaatacctttgatctaagggttcagcctttcaatgtgacacaaggaaagtattctacagctcaagactgcagtgcagatgacgacaacttccttgtgcccatagcggtgggagctgccttggcaggagtacttattctagtgttgctggcttattttattggtctcaagcaccatcatgctggatatgagcaattttag(seq id no:2);
9、(b)根据目标基因设计如seq id no:3所示的shrna序列(ccagctcctttatcaagca),将所述g3-c12-lamp2b融合基因序列与shrna序列克隆到pet-28a(+)载体上,得到共表达g3-c12-lamp2b融合蛋白和rad 51sirna的重组质粒pet-28(+)-g3-c12-lamp2b-shrna;
10、(2)利用电激转化方法将pet-28(+)-g3-c12-lamp2b-shrna重组质粒转化到克劳氏芽胞杆菌感受态细胞,涂布于含卡那霉素的na板上培养,筛选具有卡那霉素抗性的菌株,在含卡那霉素的nb液体培养基中扩大培养,将菌液离心,收集上清,超滤浓缩,超高速离心,所得沉淀重悬于pbs溶液,即得。
11、本发明还提供所述工程化克劳氏芽孢杆菌胞外囊泡在制备治疗癌症的药物中的应用。
12、作为优选,所述癌症包括但不限于胰腺癌、甲状腺癌、肾透明细胞癌、子宫内膜样腺癌、前列腺癌、头颈部鳞状细胞癌。
13、作为优选,所述工程化克劳氏芽孢杆菌胞外囊泡作为药物载体共载用于治疗癌症的化疗药物和/或核酸药物。
14、作为更优选,所述化疗药物为抑制剂olaparib。
15、本发明还提供一种药物递送载体,其包括所述工程化克劳氏芽孢杆菌胞外囊泡,所述抑制剂olaparib负载于其上构建一种药物递送系统(ebevs-ola)。
16、作为优选,所述工程化克劳氏芽孢杆菌胞外囊泡和抑制剂olaparib的质量比为20:1-100。
17、本发明还提供所述药物递送载体在制备治疗癌症的药物中的应用。
18、作为优选,所述癌症包括但不限于胰腺癌、甲状腺癌、肾透明细胞癌、子宫内膜样腺癌、前列腺癌、头颈部鳞状细胞癌。
19、作为优选,所述药物递送载体共载用于治疗癌症的化疗药物和/或核酸药物。
20、作为更优选,所述化疗药物为抑制剂olaparib。
21、与现有技术相比,本发明的有益效果在于:本发明通过基因工程设计重组质粒pet-28(+)-g3-c12-lamp2b-shrna,转化入b.clausii后实现共表达,获取携带rad51 sirna且表面表达g3-c12的ebevs,将ola负载于ebevs构建一种药物递送系统ebevs-ola,给药方式灵活,可通过口服或注射给药。本发明的工程化克劳氏芽孢杆菌胞外囊泡或药物递送载体用于制备治疗癌症的药物,利用g3-c12主动靶向并浓集于原发瘤及转移瘤,且通过膜融合实现ola和rad51sirna的胞内释放,rad51 sirna特异性沉默rad51,ola同步作用于parp酶,联合抑制dna损伤修复,产生“合成致死”作用,显著提升基于ola的维持疗法在治疗胰腺癌、甲状腺癌、肾透明细胞癌、子宫内膜样腺癌、前列腺癌、头颈部鳞状细胞癌等恶性肿瘤中的应用和疗效,从而有效延长患者生存期,具有重要的临床应用价值。
本文地址:https://www.jishuxx.com/zhuanli/20241106/325134.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。