免疫调节三特异性T细胞接合器融合蛋白的制作方法
- 国知局
- 2024-10-09 15:06:16
背景技术:
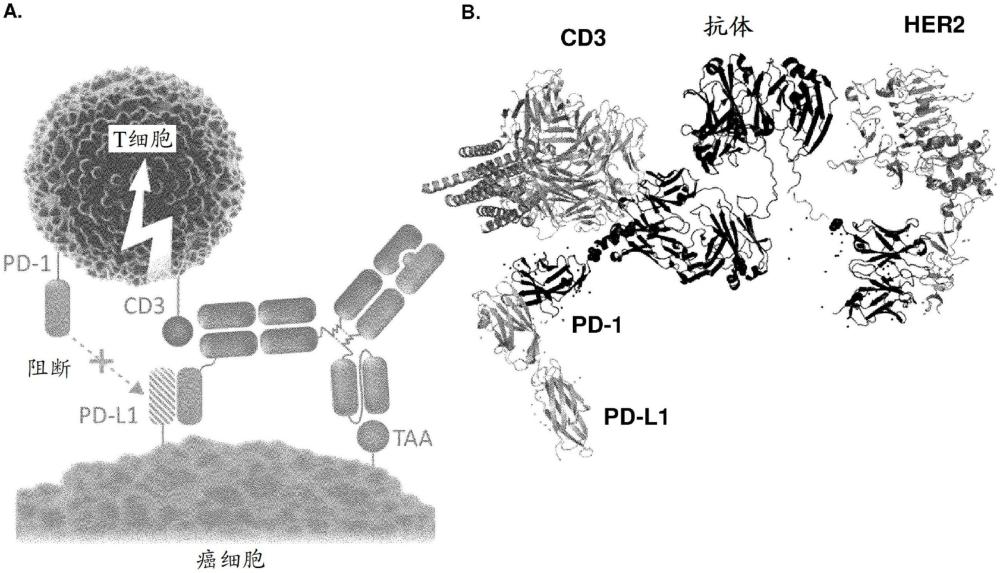
1、用于癌症治疗的检查点抑制剂诸如pd-1和pd-l1抑制剂通过阻断t细胞和癌细胞上表达的免疫检查点蛋白的相互作用来发挥其作用,从而改善否则会发生的免疫阻抑。几种抗pd-1抗体(诸如帕博利珠单抗(pembrolizumab)和纳武单抗(nivolumab))和抗pd-l1抗体(例如,阿替利珠单抗(atezolizumab))已被批准作为某些类型癌症的治疗剂。这些检查点抑制剂可以单独施用,或者连同针对在癌细胞上过表达的抗原的另一种抗体一起施用,例如与抗her2抗体组合施用。
技术实现思路
1、在某些实施方案中,本文描述了一种三特异性融合蛋白,其包含:(i)能够结合细胞毒性效应细胞表面上的cd3的第一结合结构域;(ii)能够结合肿瘤细胞表面上的肿瘤相关抗原(taa)的第二结合结构域;(iii)能够结合肿瘤细胞表面上的pd-l1的第三结合结构域;和(iv)支架,其中所述第一结合结构域、所述第二结合结构域和所述第三结合结构域与所述支架可操作地连接。此类三特异性融合蛋白可以是三价的或四价的,即它可以包含另一个结合结构域,例如第二抗taa结合结构域。
2、在一些实施方案中,本文描述了一种四价三特异性融合蛋白,其包含:(i)能够结合细胞毒性效应细胞表面上的cd3的第一结合结构域;(ii)能够结合肿瘤细胞表面上的肿瘤相关抗原(taa)的第二结合结构域和第三结合结构域;(iii)能够结合肿瘤细胞表面上的pd-l1的第四结合结构域;和(iv)支架,其中所述第一结合结构域、所述第二结合结构域、所述第三结合结构域和所述第四结合结构域与所述支架可操作地连接。
3、如本文进一步描述的,本公开的三特异性融合蛋白可以具有多种不同的型式,并且此类融合蛋白可以包含一个或多个能够将融合蛋白可以包含的各种多肽和结构域相互连接的肽接头部分。
4、在一些实施方案中,本文提供了三特异性融合蛋白,所述三特异性融合蛋白包含:抗cd3结合结构域,其包含特异性结合t细胞表面上的cd3(分化簇3)抗原的vh区和vl区;一个或两个抗taa结合结构域,其包含特异性结合肿瘤细胞表面上的taa(肿瘤相关抗原)的vh区和vl区;能够结合肿瘤细胞表面上的pd-l1受体的pd-1多肽;其中抗cd3结构域、抗taa结构域和pd-1多肽与支架可操作地连接。支架可以是抗体或其部分,并且可以具有、包含异源二聚免疫球蛋白(ig)fc区或由其组成。
5、在某些实施方案中,抗cd3结合结构域具有fab型式,抗taa结合结构域具有scfv型式,并且pd-1多肽经由肽接头融合到抗cd3结合结构域fab的vh的n末端。在某些实施方案中,抗cd3结合结构域具有fab型式,抗taa结合结构域具有scfv型式,并且pd-1多肽经由肽接头融合到抗cd3结合结构域fab的vl的n末端。
6、在某些实施方案中,本文所述的融合蛋白中使用的pd-1多肽是野生型pd-1。在某些实施方案中,pd-1多肽包含一个或多个增加或降低其对pd-l1的结合亲和力的突变,其中此类一个或多个突变(例如,氨基酸取代)是相对于某种野生型或未突变的pd-1多肽氨基酸序列而言的。在某些实施方案中,本文融合蛋白的pd-1多肽对pd-l1的亲和力为约100μm至约10pm,或约10μm至约150pm,或约100nm至约150pm。
7、在某些实施方案中,本文所述的三特异性融合蛋白包含:抗cd3结合结构域,其包含特异性结合t细胞表面上的cd3(分化簇3)抗原的vh区和vl区;一个或两个抗taa结合结构域,其包含特异性结合肿瘤细胞表面上的taa(肿瘤相关抗原)的vh区和vl区;和能够结合肿瘤细胞表面上的pd-l1受体的pd-1多肽;其中所述融合蛋白具有本文图3a-3ll中例示的型式之一的型式。
8、在一些实施方案中,taa可以是间皮素(msln)、紧密连接蛋白18.2(cldn18.2)、gpc3、dll3、psma、muc17、liv1、ror1和egfrviii中的任何一种。
9、在一些实施方案中,肽接头选自seq id no:15、16、17、18、19和20。
10、在一些实施方案中,三特异性融合蛋白减少或抑制位于t细胞上的pd-1多肽与位于癌细胞上的pd-l1多肽的结合。
11、本文还提供了本文所述的三特异性融合蛋白的药物配制物/组合物。
12、本文还提供了治疗有需要的受试者的癌症的方法,其包括向所述受试者施用所述三特异性融合蛋白。
13、本文还提供了克服或防止t细胞耗竭的方法,其包括将t细胞暴露于本文所述的三特异性融合蛋白,其中t细胞可以位于受试者,诸如人或啮齿动物体内。
技术特征:1.一种三特异性融合蛋白,其包含:
2.一种三特异性融合蛋白,其包含:
3.如权利要求1-2中任一项所述的三特异性融合蛋白,其中所述第三结合结构域与(i)所述第一结合结构域、(ii)所述第二结合结构域或(iii)所述支架连接。
4.一种三特异性融合蛋白,其包含:
5.一种三特异性融合蛋白,其包含:
6.一种三特异性融合蛋白,其包含:
7.如权利要求1-6中任一项所述的三特异性融合蛋白,其中:
8.一种三特异性融合蛋白,其包含:
9.如权利要求1-8中任一项所述的三特异性融合蛋白,其中所述支架包含二聚fc结构域或由二聚fc结构域组成,所述二聚fc结构域包含第一fc多肽和第二fc多肽。
10.如权利要求9所述的三特异性融合蛋白,其中所述二聚fc结构域是异源二聚fc结构域,并且其中所述第一fc多肽的氨基酸序列与所述第二fc多肽的氨基酸序列有至少一个氨基酸残基不同。
11.如权利要求9-10中任一项所述的三特异性融合蛋白,其中所述第一结合结构域经由第一接头fc与所述第一fc多肽连接。
12.如权利要求9-11中任一项所述的三特异性融合蛋白,其中所述第二结合结构域经由第二接头fc与所述第二fc多肽连接。
13.如权利要求11-12中任一项所述的三特异性融合蛋白,其中所述第一接头fc、所述第二接头fc或两者包含igg铰链区或其部分或变体或由igg铰链区或其部分或变体组成。
14.如权利要求11-13中任一项所述的三特异性融合蛋白,其中所述第一接头fc、所述第二接头fc或两者包含与seq id no:50中所示的氨基酸序列或其片段具有至少80%、90%或95%序列同一性的氨基酸序列或由所述氨基酸序列组成。
15.如权利要求1-14中任一项所述的三特异性融合蛋白,其中所述第一结合结构域是fab结构域并且经由所述fab重链的c末端与所述第一fc多肽的n末端连接。
16.如权利要求1-15中任一项所述的三特异性融合蛋白,其中所述第二结合结构域是scfv结构域并且经由其c末端与所述第二fc多肽的n末端连接。
17.如权利要求1-16中任一项所述的三特异性融合蛋白,其中所述三特异性融合蛋白包含三条多肽链或由三条多肽链组成,所述三条多肽链包括两条免疫球蛋白g重链和一条免疫球蛋白轻链,其中所述第一重链从n末端至c末端包含与所述第一fc多肽的ch2结构域和ch3结构域连接的fab vh和ch1结构域,所述第二重链从n末端至c末端包含与所述第二fc多肽的ch2结构域和ch3结构域连接的scfv vh和vl结构域或vl和vh结构域,并且所述轻链从n末端至c末端包含fab vl和cl结构域,其中所述轻链能够与所述第一重链的所述fab vh和ch1结构域形成fab结构域。
18.如权利要求1-17中任一项所述的三特异性融合蛋白,其中所述第三结合结构域包含pd-1多肽。
19.如权利要求1-18中任一项所述的三特异性融合蛋白,其中所述第三结合结构域由pd-1多肽组成。
20.如权利要求18-19中任一项所述的三特异性融合蛋白,其中所述pd-1多肽是野生型pd-1多肽,所述野生型pd-1多肽包含seq id no:7中所示的氨基酸序列或其片段的一部分或由所述氨基酸序列或其片段的一部分组成。
21.如权利要求18-19中任一项所述的三特异性融合蛋白,其中所述pd-1多肽与相应的野生型pd-1多肽相比包含一个或多个氨基酸修饰,当与所述相应的野生型pd-1多肽与pd-l1的结合亲和力相比时,所述一个或多个修饰增加或降低所述pd-1多肽与pd-l1的结合亲和力。
22.如权利要求21所述的三特异性融合蛋白,其中所述一个或多个氨基酸修饰包括一个或多个氨基酸取代。
23.如权利要求22所述的三特异性融合蛋白,其中所述pd-1多肽对pd-l1的结合亲和力为约100μm至约10pm、约10μm至约150pm、约100nm至150pm、或约5nm至约90nm。
24.如权利要求18-23中任一项所述的三特异性融合蛋白,其中所述pd-1多肽包含与seq id no:9或10中所示的氨基酸序列具有至少约80%、90%、95%、99%或100%序列同一性的氨基酸序列或由所述氨基酸序列组成。
25.如权利要求1-24中任一项所述的三特异性融合蛋白,其中所述抗cd3结合结构域包含vh结构域和vl结构域,所述vh结构域包含选自rstmh(seq id no:207)、yygms(seq idno:303)、kyamn(seq id no:224)和tyamn(seq id no:232)的hcdr1序列,选自yinpssaytnynqkfkd(seq id no:208)、si tssggriyypdsvkg(seq id no:301)、sitrsggriyypdsvk g(seq id no:217)、rirskynnyatyyadsvkd(seq id no:225)和rirskynnyatyyadsvkg(seq id no:233)的hcdr2序列,和选自pqvhydyngfpy(seq id no:209)、dgrdgwv ay(seq id no:275)、hgnfgnsyisyway(seq id no:226)和hgnfgnsyvswfay(seq id no:234)的hcdr3序列;所述vl结构域包含选自sasssvsymn(seq id no:211)、krntgni gsnyvn(seq id no:287)、tgntgnigsnyvn(seq id no:220)、gsstgavtsgnypn(seqid no:228)和gsstgavttsny an(seq id no:236)的lcdr1序列,选自dssklas(seq id no:212)、rndkrpd(seq id no:298)、rddkrps(seq id no:221)、gtkflap(seq id no:229)、rsyqrps(seq id no:199)和gtnkrap(seq id no:237)的lcdr2序列,和选自qqw srnppt(seq id no:214)、qsyssgfi(seq id no:295)、vl wysnrwv(seq id no:230)、atwddsldgwv(seq id no:200)和alwysnlwv(seq id no:238)的lcdr3序列。
26.如权利要求1-25中任一项所述的三特异性融合蛋白,其中所述抗cd3结合结构域包含vh结构域和vl结构域,所述vh结构域包含与seq id no:2、215、223和231中任一者所示的序列具有至少约90%、95%、97%、99%或100%序列同一性的氨基酸序列,所述vl结构域包含与seq id no:1、219、227和235中任一者所示的序列具有至少约90%、95%、97%、99%或100%序列同一性的氨基酸序列。
27.如权利要求1-26中任一项所述的三特异性融合蛋白,其中所述taa不是her2。
28.如权利要求1-27中任一项所述的三特异性融合蛋白,其中所述taa是cldn18.2。
29.如权利要求1或3-27中任一项所述的三特异性融合蛋白,其中所述taa是her2并且所述第二结合结构域的抗her2 vh序列包含:包含dtyih(seq id no:121)的hcdr1序列、包含riyptngytryadsvkg(seq id no:122)的hcdr2序列和包含wggdgfyamdy(seq id no:123)的hcdr3序列,并且所述第二结合结构域的抗her2 vl序列包含:包含rasqdvntava(seq idno:125)的lcdr1序列、包含sasflys(seq id no:126)的lcdr2序列和包含qqhyttppt(seqid no:127)的lcdr3序列。
30.如权利要求1-27中任一项所述的三特异性融合蛋白,其中所述taa是msln并且所述第二结合结构域的抗msln vh序列包含:包含gytmn(seq id no:286)的hcdr1序列、包含litpyngassynqkfrg(seq id no:288)的hcdr2序列和包含ggydgrgfdy(seq id no:285)的hcdr3序列,并且所述第二结合结构域的抗msln vl序列包含:包含sasssvsymh(seq id no:300)的lcdr1序列、包含dtsklas(seq id no:279)的lcdr2序列和包含qqwsgyplt(seq idno:294)的lcdr3序列。
31.如权利要求28所述的三特异性融合蛋白,其中所述taa是cldn18.2并且所述第二结合结构域的抗cldn18.2 vh序列包含:包含snpmi(seq id no:310)的hcdr1序列、包含iidtdgstyyadwakg(seq id no:311)的hcdr2序列和包含rlhgssngyyddl(seq id no:312)的hcdr3序列,并且所述第二结合结构域的抗cldn18.2 vl序列包含:包含qasqsiysyls(seqid no:313)的lcdr1序列、包含kastlas(seq id no:314)的lcdr2序列和包含qqgytvtnvdknt(seq id no:315)的lcdr3序列。
32.如权利要求31所述的三特异性融合蛋白,其中所述第二结合结构域的所述抗cldn18.2 vh序列包含与seq id no:316中所示的序列具有至少约90%、95%、97%、99%或100%序列同一性的氨基酸序列,并且所述第二结合结构域的所述抗cldn18.2 vl序列包含与seq id no:317中所示的序列具有至少约90%、95%、97%、99%或100%序列同一性的氨基酸序列。
33.如权利要求9-32中任一项所述的三特异性融合蛋白,其中所述第一fc多肽和所述第二fc多肽各自包含ch2结构域,所述ch2结构域包含与seq id no:6中所示的序列具有至少约90%、95%、97%、99%或100%序列同一性的氨基酸序列。
34.如权利要求9-33中任一项所述的三特异性融合蛋白,其中所述第一fc多肽或所述第二fc多肽中的一者包含含有与seq id no:4中所示序列具有至少约90%、95%、97%、99%或100%序列同一性的氨基酸序列的ch3结构域,并且另一fc多肽包含含有与seq idno:5中所示序列具有至少约90%、95%、97%、99%或100%序列同一性的氨基酸序列的ch3结构域。
35.如权利要求1或5-8中任一项所述的三特异性融合蛋白,其中所述taa是her2并且其中所述三特异性融合蛋白包含(i)与23734中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的第一重链,(ii)与21490中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的第二重链,和(iii)与12985中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的轻链。
36.如权利要求1-2或5-8中任一项所述的三特异性融合蛋白,其中所述taa是msln并且所述三特异性融合蛋白包含(i)与29207、29208、29276、29238、29282、22080或23734中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的第一重链,(ii)与23867、23270、29275或25095中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的第二重链,和(iii)与16412、23570或12985中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的轻链。
37.如权利要求1-8中任一项所述的三特异性融合蛋白,其中所述taa是cldn18.2并且所述三特异性融合蛋白包含(i)与29241、29238、29208或29211中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的第一重链,(ii)与29264、29261、29267或28373中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的第二重链,和(iii)与16412中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的轻链。
38.一种三特异性融合蛋白,其包含:
39.一种四价三特异性融合蛋白,其包含:
40.如权利要求39所述的四价三特异性融合蛋白,其中所述支架包含二聚fc结构域或由二聚fc结构域组成,所述二聚fc结构域包含第一fc多肽和第二fc多肽。
41.如权利要求40所述的四价三特异性融合蛋白,其中所述二聚fc结构域是异源二聚fc结构域,其中所述第一fc多肽的氨基酸序列与所述第二fc多肽的氨基酸序列有至少一个氨基酸残基不同。
42.如权利要求39-41中任一项所述的四价三特异性融合蛋白,其中:
43.如权利要求39-42中任一项所述的四价三特异性融合蛋白,其中(i)所述第一结合结构域是fab结构域,(ii)所述第二结合结构域是第一scfv结构域,并且(iii)所述第三结合结构域是第二scfv结构域。
44.如权利要求39-43中任一项所述的四价三特异性融合蛋白,其中所述第一结合结构域与所述第一fc多肽的n末端连接,并且所述第二结合结构域与所述第二fc多肽的n末端连接。
45.如权利要求39-44中任一项所述的四价三特异性融合蛋白,其中所述第三结合结构域与(i)所述第一结合结构域、(ii)所述第二结合结构域或(iii)所述支架连接。
46.如权利要求39-45中任一项所述的四价三特异性融合蛋白,其中:
47.如权利要求39-46中任一项所述的四价三特异性融合蛋白,其中所述第二结合结构域和所述第三结合结构域能够结合同一taa。
48.如权利要求39-47中任一项所述的四价三特异性融合蛋白,其中所述taa是msln并且所述三特异性融合蛋白包含(i)与29257或29283中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的第一重链,(ii)与23867、29258、29264、23867、29263、29267或29261中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的第二重链,和(iii)与16412、29226或29220中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的轻链。
49.如权利要求39-47中任一项所述的四价三特异性融合蛋白,其中所述taa是cldn18.2并且所述三特异性融合蛋白包含(i)与29244中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的第一重链,(ii)与29245、29248、29251或29254中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的第二重链,和(iii)与16412中所示的克隆序列具有至少90%、95%、97%、99%或100%序列同一性的轻链。
50.如权利要求1-49中任一项所述的三特异性融合蛋白,其中在与所述细胞毒性效应细胞上的cd3、肿瘤细胞上的所述taa和肿瘤细胞上的pd-l1结合时,所述三特异性融合蛋白形成能够诱导效应细胞介导的针对所述肿瘤细胞的细胞毒性的tcr非依赖性免疫突触。
51.如权利要求1-50中任一项所述的三特异性融合蛋白,其中所述三特异性融合蛋白结合同一肿瘤细胞上的所述taa和所述pd-l1。
52.如权利要求1-51中任一项所述的三特异性融合蛋白,其中所述三特异性融合蛋白结合不同肿瘤细胞上的所述taa和所述pd-l1。
53.如权利要求1-52中任一项所述的三特异性融合蛋白,其中当与型式匹配的双特异性抗taa/抗cd3抗体与抗pd-l1抗体的组合相比时,所述三特异性融合蛋白能够以约1.1倍至约2倍、或约1.2倍至约1.7倍的效率阻断免疫细胞与肿瘤细胞之间的pd-1:pd-l1检查点。
54.如权利要求1或权利要求38所述的三特异性融合蛋白,其中所述三特异性融合蛋白:
55.一种药物组合物,其包含权利要求1-54中任一项所述的三特异性融合蛋白,以及药学上可接受的载剂、赋形剂、稀释剂或它们的组合。
56.一种核酸分子或核酸分子集合,其编码权利要求1-54中任一项所述的三特异性融合蛋白。
57.一种载体或载体集合,其包含权利要求56所述的核酸分子或核酸分子集合。
58.一种细胞,其包含权利要求56所述的核酸分子或核酸分子集合,或权利要求57所述的载体或载体集合。
59.一种产生权利要求1-54中任一项所述的三特异性融合蛋白的方法,所述方法包括:
60.如权利要求59所述的方法,其还包括在步骤(b)之后,纯化所述三特异性融合蛋白。
61.一种在包含细胞毒性效应细胞和肿瘤细胞的细胞群体中引发抗肿瘤免疫反应的方法,所述方法包括将所述细胞群体与有效量的权利要求1-54中任一项所述的三特异性融合蛋白接触,其中所述细胞毒性效应细胞表达cd3,并且所述肿瘤细胞表达taa和pd-l1。
62.一种抑制表达taa和pd-l1的肿瘤细胞增殖的方法,所述方法包括将包含肿瘤细胞和细胞毒性效应细胞的细胞群体与有效量的权利要求1-54中任一项所述的三特异性融合蛋白接触,其中所述细胞毒性效应细胞表达cd3。
63.一种杀伤表达taa和pd-l1的肿瘤细胞的方法,所述方法包括将包含肿瘤细胞和细胞毒性效应细胞的细胞群体与有效量的权利要求1-54中任一项所述的三特异性融合蛋白接触,其中所述细胞毒性效应细胞表达cd3。
64.如权利要求61-63中任一项所述的方法,其中所述taa和所述pd-l1位于同一肿瘤细胞上。
65.如权利要求61-63中任一项所述的方法,其中所述taa和所述pd-l1位于不同肿瘤细胞上。
66.如权利要求61-65中任一项所述的方法,其中cd3、所述taa和所述pd-l1的结合在所述免疫细胞和所述肿瘤细胞之间形成tcr非依赖性人工免疫突触,从而引发所述免疫细胞针对所述肿瘤细胞的细胞毒性免疫反应。
67.如权利要求61-66中任一项所述的方法,其中所述细胞群体位于活的受试者中。
68.一种治疗有需要的受试者的癌症的方法,所述方法包括向所述受试者施用权利要求1-54中任一项所述的三特异性融合蛋白。
69.如权利要求68所述的方法,其中所述三特异性融合蛋白引发针对所述受试者中的所述癌症的细胞毒性免疫反应,从而治疗所述受试者中的所述癌症。
70.如权利要求67-69中任一项所述的方法,其中所述受试者是啮齿动物、非人灵长类动物或人。
71.如权利要求1-54中任一项所述的三特异性融合蛋白,其用于在癌症治疗中使用。
72.如权利要求1-54中任一项所述的三特异性融合蛋白在制造用于癌症治疗的药物中的用途。
73.一种包含三特异性融合蛋白的药物组合物,所述三特异性融合蛋白包含:
74.一种治疗有需要的受试者的疾病的方法,所述方法包括向所述受试者施用三特异性融合蛋白,所述三特异性融合蛋白包含:
75.一种杀伤有需要的受试者中的癌细胞的方法,所述方法包括向所述受试者施用三特异性融合蛋白,所述三特异性融合蛋白包含:
技术总结本公开提供了具有用于程序性靶标接合的多功能生物设计的融合蛋白。在某些实施方案中,本文所述的融合蛋白提供了同时的T细胞和靶抗原接合以及免疫检查点靶向。技术研发人员:S·B·迪克西特,E·埃斯科巴-卡布雷拉,F·海因克尔,A·范罗苏姆,H·普拉塔普,M·波芬博格,C·L·皮希特里,M·M·弗斯特雷特受保护的技术使用者:酵活英属哥伦比亚有限公司技术研发日:技术公布日:2024/9/29本文地址:https://www.jishuxx.com/zhuanli/20241009/307637.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表