慢性炎症的诊断和治疗的制作方法
- 国知局
- 2024-10-21 14:27:18
本技术涉及生物医药领域,具体涉及慢性炎症的诊断和治疗。
背景技术:
1、机体在感染微生物后或收到组织损伤等情况下引起体液中多种细胞因子如tnf、il-6、il-8、il-12、ifn-γ和mcp-1等迅速并大量产生,甚至可能引起细胞因子风暴以及急性呼吸窘迫综合症、多器官衰竭等多种严重的临床疾病。炎症因子与各类急性及慢性炎症疾病密切相关。而目前为止,针对这些疾病在临床上并没有有效的治疗方法。
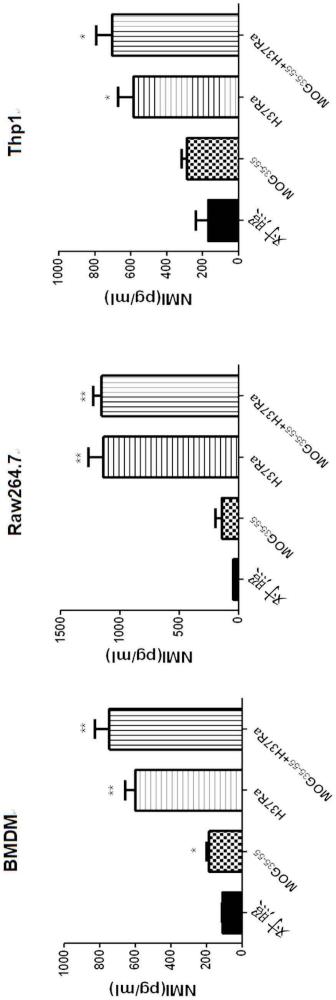
2、有生存压力的细胞会释放内源性细胞因子,启动免疫应答反应,发挥有效清除受损伤或被感染的细胞的作用。在组织感染或损伤时,一类被称为损伤相关分子模式(damps)的细胞因子释放并激活邻近的吞噬细胞,最终清除丧失正常功能的细胞。damp可以启动天然免疫应答并加剧炎症反应,进而对抗感染和细胞损伤。因此,damp的鉴定和其功能的揭示至关重要。在过去,本技术发明人发现两个可以作为da mps发挥作用的蛋白,即n-myc和stat相互作用蛋白(nmi)和干扰素诱导蛋白35(ifp35)。研究发现,ifp35和nmi可以在被lps或者干扰素激活后一小时内,被单核细胞和巨噬细胞分泌到细胞外,并在脂多糖诱导的脓毒症模型或对乙酰氨基酚诱发的肝损伤模型中,被活化的巨噬细胞释放。胞外nmi和ifp35可以通过toll样受体4(tlr4)激活nf-κb进而激活巨噬细胞并释放促炎性细胞因子。此外,在死于严重炎症反应的患者血清中,nmi的水平显著升高。nmi缺失可减轻炎症反应,并降低脓毒症模型和肝损伤模型中小鼠的死亡率。针对ifp35的抗体可以降低炎症因子的表达水平,从而有效提高败血病小鼠的存活率。
3、以多发性硬化症(multiple sclerosis,ms)为例。多发性硬化是慢性炎症疾病中的一种。ms可引起患者感觉、精神、运动、肢体活动和认知功能障碍,是引起青壮年人口致残的主要原因之一。
4、ifp35蛋白家族包含两种同源蛋白:n-myc和stat相互作用蛋白(nmi)和干扰素诱导蛋白35(ifp 35),它们都是干扰素诱导基因(isgs),人体机体及免疫细胞在受到干扰素诱导后,细胞中的表达量会升高。此外,它们还是损伤相关分子模式(damp),在感染或器官损伤中,nmi和ifp35可以被激活的巨噬细胞释放,通过tlr4受体信号通路激活nf-κb,促进巨噬细胞释放促炎细胞因子,nmi和ifp35敲除可以降低小鼠由于细菌或病毒感染导致的脓毒症和肝损伤模型的死亡率。lps、沙门氏菌等病菌、病毒等诱导的小鼠败血症小鼠模型以及由于毒性物质(如对乙酰氨基酚apap)侵入体内的小鼠动物模型中,nmi和ifp35能够由细胞内快速释放到血清等体液中。注射ifp35保护性抗体,能够保护lps和沙门氏菌、以及apap对小鼠造成的机体损伤。
5、在难以开发出有效的特异性抗病毒药物的情况下,控制病毒感染患者体内的过度炎症反应对减轻机体炎性损伤及降低死亡率尤为重要。找到导致炎症因子风暴的关键细胞因子,开发新型诊疗药物对于应对突发病毒性疾病十分必要。
6、与sars病毒、流感病毒和其它呼吸道病毒类似,covid-19病毒感染的靶器官为肺脏,可造成感染患者肺衰竭并导致急性呼吸窘迫综合征。病毒感染宿主后,往往导致病患体内发生强烈的或失调的炎症反应。炎症失调和炎症过度被认为是sars等病毒致死的重要原因,推测这也是covid-19病毒感染致死的重要原因。因此,病毒感染疾病需要从两方面进行治疗:一方面是直接的抗病毒药物治疗;另一方面则是需要平衡机体的免疫反应,抑制免疫过度。在没有针对性的抗病毒药物的情况下,调控机体的炎症反应对减轻疾病损伤程度、降低死亡率尤其重要,临床上迫切需要研发精准调控炎症反应的药物。
7、炎症反应涉及各类免疫细胞和大量炎症相关细胞因子的参与,是一个被精确调控的过程。炎症反应是一把双刃剑。一方面它是机体免疫防御的重要途径,用以清除感染。另一方面,炎症失调是很多疾病发生的重要原因,如脓毒症、慢性炎症疾病及自身免疫性疾病等。病原侵染情况下,宿主的免疫系统产生内源性的损伤相关分子模式(damageassociated molecular pattern,damp)。目前人体中发现了几种damp类炎症因子,包括hmgb1、il1b、il33、s100a等。damp作为炎症因子进一步被细胞的模式识别受体(如tlr4等)识别,激活天然免疫细胞下游信号通路(包括jak-stat通路等),激活细胞中炎症相关的转录因子,如nf-κb和irf3/7等,诱导大量炎症相关基因的转录与表达,激活免疫反应。所以,damp炎症因子是免疫系统中一类非常重要的炎症反应分子。这些damp类炎症因子普遍被应用于临床检测及作为抗体、小分子化药等药物研发的靶标。
8、目前,针对爆发的covid-19病毒感染,尚缺乏临床确定有效的疫苗和抗病毒药物。根据报道,一些抗hiv及sars/mers的药物,如洛匹那韦、瑞德西韦(remdesivir)等可能在covid-19病毒感染病例中产生治疗效果。临床上,以往治疗sars以及目前的covid-19病毒感染的危重症患者时中采取的措施会包括大剂量使用激素类药物控制过度炎症反应。但是,大量的激素使用往往带来严重的副作用,过度的免疫抑制也不利于机体清除病毒。因此,寻找关键的调控炎症反应细胞因子,筛选能够有效抑制导致宿主过度炎症反应的细胞因子药物是解决新发、突发传染病的有效治疗手段,可用于临床及预后的精准干预治疗。这不仅对目前的covid-19病毒的防治具有重要意义,且在未来应对各类缺乏针对性药物的突发传染性疾病也具有普遍的意义。
技术实现思路
1、本技术所要解决的技术问题之一是,提供一种预防和/或治疗慢性炎症疾病的方法和产品及相关抗体,以及提供一种诊断慢性炎症疾病的方法和产品及相关抗体。
2、本技术提供了试剂在制备预防和/或治疗慢性炎症疾病的产品中的应用的技术方案。
3、该技术方案如下:
4、试剂在制备预防和/或治疗慢性炎症疾病的药物中的应用;所述试剂为如下中的至少一种:
5、(1)抑制被分泌到细胞外作为炎症因子的异常含量的ifp35和/或nmi的活性的物质;
6、(2)抑制被分泌到细胞外作为炎症因子的ifp35和/或nmi的含量和/或活性的物质;
7、(3)抑制ifp35和/或nmi被分泌到细胞外作为炎症因子的物质;
8、(4)抑制ifp35和/或nmi的含量和/或活性的异常增高的物质;
9、(5)抑制ifp35和/或nmi被分泌到细胞外的物质;
10、(6)抑制ifp35和/或nmi作为炎症因子引起慢性炎症疾病的物质或抑制ifp35和/或nmi作为da mps引起慢性炎症疾病的物质;
11、(7)抑制ifp35和/或nmi上调一些炎症因子的表达和分泌的物质;所述一些炎症因子为干扰素、tnf、il1和/或il6;
12、(8)抑制ifp35和/或nmi与tlr4作用通过tlr4/md2激活nf-κb的物质。
13、本技术提供了一种预防和/或治疗慢性炎症疾病的方法。
14、本技术所提供的预防和/或治疗慢性炎症疾病的方法,包括如下步骤,向生物体施加有效量的如下试剂,以达到预防和/或治疗慢性炎症疾病的目的;
15、所述试剂为如下中的至少一种:
16、(1)抑制被分泌到细胞外作为炎症因子的异常含量的ifp35和/或nmi的活性的物质;
17、(2)抑制被分泌到细胞外作为炎症因子的ifp35和/或nmi的含量和/或活性的物质;
18、(3)抑制ifp35和/或nmi被分泌到细胞外作为炎症因子的物质;
19、(4)抑制ifp35和/或nmi的含量和/或活性的异常增高的物质;
20、(5)抑制ifp35和/或nmi被分泌到细胞外的物质;
21、(6)抑制ifp35和/或nmi作为炎症因子引起慢性炎症疾病的物质或抑制ifp35和/或nmi作为da mps引起慢性炎症疾病的物质;
22、(7)抑制ifp35和/或nmi上调一些炎症因子的表达和分泌的物质;所述一些炎症因子为干扰素、tnf、il1和/或il6;
23、(8)抑制ifp35和/或nmi与tlr4作用通过tlr4/md2激活nf-κb的物质。
24、现有技术中任何能够实现上述(1)-(8)任一所述功能的试剂在制备预防和/或治疗慢性炎症疾病的产品中的应用都属于本技术的保护范围。
25、上述(1)-(5)中的抑制,可以是直接抑制,比如直接抑制ifp35和/或nmi的含量和/或活性的异常增高,或直接抑制被分泌到细胞外作为炎症因子的异常含量的ifp35和/或nmi的活性,比如直接抑制if p35和/或nmi被分泌到细胞外作为炎症因子,比如抑制被分泌到细胞外作为炎症因子的ifp35和/或nmi的含量和/或活性;也可以是间接地通过抑制干扰素的表达和/或活性进行抑制ifp35和/或nmi。
26、上述治疗方法和治疗应用中,所述试剂为如下中至少一种:
27、抗体或多肽或抗原结合片段,其特异结合ifp35和/或nmi,其具有上述(1)-(8)至少一种功能;
28、小分子化合物,其具有上述(1)-(8)至少一种功能;
29、核酸试剂,具有上述(1)-(8)至少一种功能。
30、核酸分子可为sirna,shrna,或mirna,可以靶向ifp35和/或nmi的编码基因的。
31、小分子化合物,可以是抑制ifp35和/或nmi的分泌、表达和/或活性的小分子化合物。
32、所述抗体或多肽或抗原结合片段可以是特异结合如下抗原表位的抗体:(1)抗原表位的序列位于seq id no:2的第81-170,177-268,或136-216位氨基酸之内;(2)抗原表位的序列位于seq id no:4第81-168,175-266,或134-214位氨基酸之内;(3)抗原表位的序列位于seq id no:6第104-193,202-293,或151-250位氨基酸之内;(4)抗原表位的序列位于seq id no:8第103-192,201-292,或151-240位氨基酸之内。
33、上述治疗方法和治疗应用中,所述抗体可为如下a或b或c或d的抗体,
34、a、该抗体、多肽或抗原结合片段特异结合ifp35/nmi的抗原表位,所述抗原表位为如下(1)或(2):所述抗原表位包含如下氨基酸位点:ifp35(seq id no:2)的arg163,asn164,arg191,gln194,ile195,gln197,phe198,thr199,pro201,gln206,pro208,arg210;(2)所述抗原表位包含如下氨基酸位点:nmi(seq id no:8)的arg185,asn186 lys215,lys218,lys219,glu221,tyr222,pro223,tyr225,cys230,arg232,thr234。
35、b、任何能够结合上述(1)中抗原表位中的至少一个氨基酸残基并抑制ifp35的活性抗体或小分子或多肽物质;
36、c、任何能够结合上述(2)中抗原表位中的至少一个氨基酸残基并抑制nmi的活性抗体或小分子或多肽物质。
37、d、所述抗体为35nidmab抗体,其具有轻链可变区和重链可变区,重链可变区中含有cdr1,cdr2和cdr3,cdr1的序列是seq id no:9的第25-32位氨基酸(gytftnyg(seq idno:13)),cdr2的序列是seq id no:9的第50-57位氨基酸(intytgep(seq id no:14)),cdr3的序列是seq id no:9的第98-106位氨基酸(ygyswamdy(seq id no:15));轻链可变区中含有cdr1,cdr2和cdr3,cdr1的序列是seq id no:10的第26-31位氨基酸(sssvsy(seq id no:16)),cdr2的序列是seq id no:10的第49-51位氨基酸(dts(seq id no:17)),cdr3的序列是seq id no:10的第90-96位氨基酸(wssnppi(seq id no:18))。
38、上述的抗体、多肽或抗原结合片段中,所述抗体为将35nidmab除cdr外其余位置氨基酸进行突变得到的抗体;或,所述抗体为将35nidmab进行人源化的抗体。
39、本领域技术人员可以根据本领域公知常识和惯用手段,将上述任一所述抗体,除了cdr序列之外的其它氨基酸进行改造突变,得到的抗体也属于本技术的保护范围。
40、所述人源化抗体为如下中至少一种:ae001-h1+l1、ae001-h2+l2或ae001-h3+l3。这三种抗体均具有轻链可变区和重链可变区,重链可变区中含有cdr1,cdr2和cdr3,cdr1的序列是seq id no:9的第25-32位氨基酸(gytftnyg),cdr2的序列是seq id no:9的第50-57位氨基酸(intytgep),cdr3的序列是seq id no:9的第98-106位氨基酸(ygyswamdy);轻链可变区中含有cdr1,cdr2和cdr3,cdr1的序列是seq id no:10的第26-31位氨基酸(sssvsy),cdr2的序列是seq id no:10的第49-51位氨基酸(dts),cdr3的序列是seq idno:10的第90-96位氨基酸(wssnppi)。
41、ae001-h1+l1的重链恒定区序列为ae001h1(seq id no:1),轻链恒定区序列为ae001l1(seq id no:3)。
42、ae001-h2+l2的重链恒定区序列为ae001h2(seq id no:5),轻链恒定区序列为ae001l2(seqid no:7)。
43、ae001-h3+l3的重链恒定区序列为ae001h3(seq id no:11),轻链恒定区序列为ae001l3(se q id no:12)。
44、上述的抗体、多肽或抗原结合片段中,所述抗体为将35nidmab或其人源化抗体中的至少一个cdr中氨基酸残基进行突变得到的抗体。
45、上述的抗体、多肽或抗原结合片段中,所述将35nidmab或其人源化抗体中的至少一个cdr进行突变为进行如下至少一种突变:
46、35nidmab的重链可变区cdr1的第25、26、27、28、29和/或32位氨基酸残基进行突变;即(25gytftnyg 32)中除了ny其余氨基酸位置进行突变。
47、35nidmab的重链可变区cdr2的第50、52、55、56和/或57位氨基酸残基进行突变;即(50int ytgep 57)中除了下划线氨基酸外其余位置的氨基酸进行突变。
48、35nidmab的重链可变区cdr3的第98、99、101、103、104、105和/或106位氨基酸残基进行突变;即(98ygyswamdy 106)中除了下划线氨基酸外其余位置的氨基酸进行突变。
49、35nidmab的轻链可变区cdr1的第26、27、28和/或29位氨基酸残基进行突变;即(26sssvsy 31)中除了下划线氨基酸外其余位置的氨基酸进行突变。
50、35nidmab的轻链可变区cdr3的第90、91、94、95和/或96位氨基酸残基进行突变;即(90wss nppi 96)中除了下划线氨基酸外其余位置的氨基酸进行突变。
51、在35nidmab的抗体重链可变区cdr1序列(25gytftnyg 32)中,与抗原结合的主要是asn30和tyr31两个氨基酸;在抗体重链可变区cdr2序列(50intytgep 57)中,与抗原结合的主要是asn51,tyr53以及thr54三个氨基酸;在抗体重链可变区cdr3(98ygyswamdy 106)序列中,与抗原结合的主要是tyr100和trp102两个氨基酸。以上所述残基可以称为抗体重链与抗原相互作用残基。其它cdr残基不与或者很少与抗原ifp35结合,因此更易进行更改而获得不显著影响抗体活性的抗体。因此更改任何以上所述cdr中不与抗原相互作用的残基,仍然可能保持与ifp35或nmi的抗原-抗体复合体结构中对应的抗原表位氨基酸结合,应在本技术保护范围内。
52、在抗体轻链可变区cdr1序列(26sssvsy 31)中,与抗原结合的主要氨基酸是ser30和tyr31;在抗体轻链可变区cdr2序列(49dts 51)中,与抗原结合的主要氨基酸是asp49;在抗体轻链可变区cdr3序列(90wssnppi 96)中,与抗原结合的主要氨基酸是ser92和asn93。以上所述残基可以称为抗体重链与抗原相互作用残基。其它cdr残基不与或者很少与抗原ifp35结合,因此更易进行更改而获得不显著影响抗体活性的抗体。因此更改任何以上所述cdr中不与抗原相互作用的残基,仍然可能保持与ifp35或nmi的抗原-抗体复合体结构中对应的抗原表位氨基酸结合,应在本技术保护范围内。
53、上述的抗体、多肽或抗原结合片段中,所述将35nidmab或其人源化抗体中的至少一个cdr进行突变为进行如下至少一种突变:
54、35nidmab的重链可变区cdr1的第30和/或31位氨基酸残基进行突变;
55、35nidmab的重链可变区cdr2的第51、53和/或54位氨基酸残基进行突变;
56、35nidmab的重链可变区cdr3的第100和/或102位氨基酸残基进行突变;
57、35nidmab的轻链可变区cdr1的第30和/或31位氨基酸残基进行突变;
58、35nidmab的轻链可变区cdr3的第92和/或93位氨基酸残基进行突变。
59、所述抗体或抗原结合片段是能够识别如下两个或以上氨基酸残基的抗体或抗原结合片段:35nidma b或其人源化抗体中的重链的asn30、tyr31、asn51、tyr53、thr54、tyr100和trp102位氨基酸残基,其参与与抗原ifp35及nmi的识别。
60、所述抗体或抗原结合片段是能够识别如下两个或以上氨基酸残基的抗体或抗原结合片段:35nidma b或其人源化抗体中的轻链的ser30、tyr31、asp49、ser92和asn93位氨基酸残基,其参与与抗原ifp35及nmi的识别。
61、在抗体重链可变区cdr1序列(25gytftnyg 32)中,与抗原结合的主要是asn30和tyr31两个氨基酸;在抗体重链可变区cdr2序列(50intytgep 57)中,与抗原结合的主要是asn51,tyr53以及thr54三个氨基酸;在抗体重链可变区cdr3(98ygyswamdy 106)序列中,与抗原结合的主要是tyr100和trp102两个氨基酸。因此,改变其中部分氨基酸都可能有利于抗原抗体的结合能力。以上所述残基可以称为抗体重链与抗原相互作用残基。更改这些与抗原相互作用残基的任何1个或2个或3个,仍然保持与ifp35或nmi的抗原-抗体复合体结构中对应的抗原表位氨基酸结合,应在本技术保护范围内。
62、在抗体轻链可变区cdr1序列(26sssvsy 31)中,与抗原结合的主要氨基酸是ser30和tyr31;在抗体轻链可变区cdr2序列(49dts 51)中,与抗原结合的主要氨基酸是asp49;在抗体轻链可变区cdr3序列(90wssnppi 96)中,与抗原结合的主要氨基酸是ser92和asn93。因此,部分这些氨基酸的改变都可能有利于抗原抗体的结合能力。以上所述残基可以称为抗体轻链与抗原相互作用残基。更改这些与抗原相互作用残基的任何1个或2个或3个,仍然保持与ifp35或nmi的抗原-抗体复合体结构中对应的抗原表位氨基酸结合,应在本技术保护范围内。
63、上述的抗体、多肽或抗原结合片段中,所述将35nidmab或其人源化抗体中的至少一个cdr进行突变得到的抗体为如下至少一种:ae001-5、ae001-6、ae001-7、ae001-8、ae001-9。
64、ae001-5、ae001-6、ae001-7、ae001-8、ae001-9的重链可变区的cdr和轻链可变区的cdr如下表所示。
65、重链可变区cdr:
66、
67、轻链可变区cdr:
68、
69、ae001-5、ae001-6、ae001-7、ae001-8、ae001-9的重链可变区和轻链可变区除cdr以外的序列,本领域技术人员可以根据自己的需要进行改造。具体的一个例子,ae001-5、ae001-6、ae001-7、ae001-8、ae001-9的重链可变区和轻链可变区除cdr以外的序列,还可以与35nidmab抗体的相应序列相同相同。
70、ae001-5、ae001-6、ae001-7、ae001-8、ae001-9的恒定区序列,本领域技术人员可以根据自己的需要进行改造。具体的一个例子,ae001-5、ae001-6、ae001-7、ae001-8、ae001-9的恒定区序列可与上述ae001-h1+l1、ae001-h2+l2或ae001-h3+l3的恒定区序列相同。
71、上述治疗方法和治疗应用中,所述慢性炎症疾病包括多发性硬化症、关节炎、类风湿关节炎、银屑病(牛皮癣)、各种肠炎(如ibd)、哮喘、慢阻肺和系统性红斑狼疮、慢性肝炎、慢性肾炎、慢性胰腺炎、脑炎、恶性肿瘤、白血病、阿尔兹海默症、帕金森综合征等。
72、上述治疗方法和治疗应用中,所述慢性炎症疾病都由分泌的异常含量ifp35/nmi炎症因子发挥作用,包括类风湿关节炎(rheumatoid arthritis(ra))、骨性关节炎(osteoarthritis(oa))、多发性硬化(multiple sclerosis,ms)、动脉粥样硬化(atherosclerosis)、心肌梗死(myocardial infarction)、慢阻肺(copd)、慢性肾炎、慢性肝炎、慢性胰腺炎、ii型糖尿病(type 2diabetes)、系统性红斑狼疮(systemic lupuserythematosus(sle))、阿兹海默(alzheimers disease)、帕金森(parkinsons disease(pd))恶性肿瘤、哮喘(asthma)、过敏性疾病(allergic diseases)、心血管疾病(cardiovascular diseases)、肌肉骨骼疾病(musculoskeletal diseases)、炎性肠炎(ibd)、肥胖及糖尿病(obesity和diabetes)、视网膜炎症疾病(amd)、牙周炎(periodontitis)、葡萄膜炎(uveitis)等。
73、慢性炎症疾病的病理过程有多种炎症因子参与。作为可以被免疫细胞等分泌到细胞外基质(血液、体液等)、发挥促进炎症反应作用的炎症因子,ifp35和/或nmi也可以被细胞分泌到细胞外基质(血液、体液等)中,发挥激活炎症反应的作用。本技术中示例性研究的多发性硬化症是慢性炎症疾病的一个典型代表。多发性硬化症的发生与小胶质细胞密切相关。小胶质细胞可以发挥部分神经系统的免疫细胞(巨噬细胞)的作用,释放炎症因子,促进炎症反应的发生。这一现象相当于机体其它组织和器官发生炎症反应时由巨噬细胞等免疫细胞引发的炎症反应。本技术的发明人发现,lps等诱导情况下小胶质细胞分泌ifp35/nmi到细胞培养基质中,且患有多发性硬化症的动物血清中ifp35/nmi含量也有所上升。表明ifp35/nm i与多发性硬化症存在着关联。总体来说,巨噬细胞、小胶质细胞等免疫细胞释放炎症因子引发炎症反应,可能导致各类慢性炎症疾病,ifp35/nmi作为其中的炎症因子。本技术还提供了诊断慢性炎症疾病的方法和应用,为如下技术方案a、b或c或d:
74、技术方案a、检测ifp35和/或nmi的物质在制备诊断慢性炎症疾病的产品中的应用;
75、所述检测ifp35和/或nmi的物质为如下至少一种:
76、(1)检测生物体脊髓组织中ifp35/nmi的表达量是否显著升高;
77、(2)检测ifp35/nmi是否被分泌到生物体的血液中或体液中(如脑脊液中);
78、(3)检测生物体的血液中或体液中(如脑脊液中)是否含有ifp35/nmi,和/或检测生物体的血液中或体液中(如脑脊液中)的ifp35/nmi的含量;
79、(4)检测被分泌到生物体的血液中或体液中(如脑脊液中)的ifp35/nmi的含量用于协助临床炎症疾病的医学诊断;
80、(5)检测分泌的ifp35/nmi与生物体中其它炎症因子(如tnf、il1、il6等)以及生物标志物降钙素原(pct)、c反应蛋白(crp)的表达提高和分泌到血液中含量增多之间的差异及相关性;
81、技术方案b、为疾病诊断应用的临床检测产品用于检测分泌到血清及体液中的ifp35和/或nmi;
82、所述检测分泌到血清及体液中的ifp35和/或nmi的临床应用产品包括如下至少一种:荧光发光临床检测试剂(盒)、化学发光临床检测试剂(盒)、elisa检测试剂(盒)、pcr临床检测试剂(盒)等。
83、检测分泌的ifp35/nmi与生物体中其它炎症因子(如tnf、il1、il6等)以及生物标志物降钙素原(pct)、c反应蛋白(crp)的表达提高和分泌到血液中含量增多之间的差异及相关性;
84、技术方案c、为慢性炎症疾病诊断应用的临床检测产品用于检测分泌到血清及体液中的ifp35和/或nmi;
85、所述检测分泌到血清及体液中的ifp35和/或nmi的临床应用产品包括如下至少一种:荧光发光临床检测试剂(盒)、化学发光临床检测试剂(盒)、elisa检测试剂(盒)、pcr临床检测试剂(盒)等。
86、检测分泌的ifp35/nmi与生物体中其它炎症因子(如tnf、il1、il6等)以及生物标志物降钙素原(pct)、c反应蛋白(crp)的表达提高和分泌到血液中含量增多之间的差异及相关性。
87、技术方案d、一种诊断待测生物体是否患有慢性炎症疾病的方法,包括如下中的至少一种的步骤:
88、(1)检测生物体组织中(如脊髓组织)中ifp35/nmi的表达量是否显著升高;
89、(2)检测ifp35/nmi是否被分泌到生物体的血液中或体液中(如脑脊液中);
90、(3)检测生物体的血液中或体液中(如脑脊液中)是否含有ifp35/nmi,和/或检测生物体的血液中或体液中(如脑脊液中)的ifp35/nmi的含量;
91、(4)检测被分泌到生物体的血液中或体液中(如脑脊液中)的ifp35/nmi的含量用于协助临床炎症疾病的医学诊断;
92、(5)检测分泌的ifp35/nmi与生物体中其它炎症因子(如tnf、il1、il6等)以及生物标志物降钙素原(pct)、c反应蛋白(crp)的表达提高和分泌到血液中含量增多之间的差异及相关性;
93、上述诊断方法和应用中,可以根据如下至少一种的判断标准来诊断待测生物体是否患有慢性炎症疾病:
94、(1)若待测生物体组织中(如脊髓组织)中ifp35/nmi的表达量显著升高,则判断待测生物体患有慢性炎症疾病;
95、(2)若检测到ifp35/nmi被分泌到生物体的血液中或体液中(如脑脊液中),则判断待测生物体患有慢性炎症疾病;
96、(3)若检测到生物体的血液中或体液中(如脑脊液中)中含有ifp35/nmi,则判断待测生物体患有慢性炎症疾病。
97、(4)ifp35/nmi表达提高与生物体中其它炎症因子(干扰素、tnf、il1、il6等)的表达和分泌到血液或体液中相一致,或具有临床表征性状,则判断待测生物体患有慢性炎症疾病。
98、上述诊断方法和应用中,所述检测分泌到血清及体液中的ifp35和/或nmi的临床应用产品包括如下至少一种:荧光发光临床检测试剂(盒)、化学发光临床检测试剂(盒)、elisa检测试剂(盒)、pcr临床检测试剂(盒)等。
99、上述诊断方法和应用中,检测ifp35和/或nmi的含量和/或活性可以从dna,rna或蛋白水平进行检测。
100、上述诊断方法和应用中,dna和/或rna水平检测可以使用特异性核酸探针,也可以使用pcr引物或芯片等。
101、上述诊断方法和应用中,蛋白水平检测用抗体。
102、上述诊断方法和应用中,目前,临床上常用的炎症疾病检测指标包括降钙素原(pct)、c反应蛋白(crp)、tnf和il6等。但是这些检测指标存在着局限性。比如pct不能用来指示由于病毒造成的感染。另外,对于不同疾病,不同的炎症因子在不同病人上表现不同。因此,一方面需要开发其它合适的检测指标;另一方面应该对已知的炎症因子进行普遍检测。对于慢性炎症疾病,临床上可以检测ifp35和nmi并与其它指标比较。
103、上述诊断方法和应用中,可以通过检测小鼠脊髓组织中ifp35/nmi的表达量是否显著升高、或者检测ifp35/nmi是否被分泌到小鼠血液中或体液中(如脑脊液中)、或者检测ifp35/nmi与小鼠中其它炎症因子(如tnf、il1、il6等)的表达提高和分泌到血液中含量增多之间的相关性,来帮助诊断小鼠是否患有ms。若小鼠组织中ifp35/nmi的表达量异常升高、ifp35/nmi并被异常分泌到小鼠血液中或体液中(如脑脊液中)、或者ifp35/nmi表达提高与小鼠中其它炎症因子(干扰素、tnf、il1、il6等)的表达和分泌到血液中相一致,造成小鼠从步态改变、四肢是否有瘫痪等外在症状十分明显,基本可以诊断小鼠患有ms。
104、上述诊断方法和应用中,所述检测物质为a或b或c或d的抗体、多肽或抗原结合片段:
105、a、该抗体、多肽或抗原结合片段特异结合ifp35/nmi的抗原表位,所述抗原表位为如下(1)或(2):所述抗原表位包含如下氨基酸位点:ifp35的arg163,asn164,arg191,gln194,ile195,gln197,phe198,thr199,pro201,gln206,pro208,arg210;(2)所述抗原表位包含如下氨基酸位点:nmi的arg185,as n186 lys215,lys218,lys219,glu221,tyr222,pro223,tyr225,cys230,arg232,thr234。
106、b、任何能够结合上述(1)中抗原表位中的至少一个氨基酸残基并抑制ifp35的活性抗体或小分子或多肽物质;
107、c、任何能够结合上述(2)中抗原表位中的至少一个氨基酸残基并抑制nmi的活性抗体或小分子或多肽物质。
108、d、为如下35nidmab抗体:
109、所述抗体具有轻链可变区和重链可变区,重链可变区包括cdr1,cdr2和cdr3,cdr1的序列是seq id no:9的第25-32位氨基酸(gytftnyg),cdr2的序列是seq id no:9的第50-57位氨基酸(intytgep),cdr3的序列是seq id no:9的第98-106位氨基酸(ygyswamdy);轻链可变区包括cdr1,cdr2和cdr3,cdr1的序列是seq id no:10的第26-31位氨基酸(sssvsy),cdr2的序列是seq id no:10的第49-51位氨基酸(dts),cdr3的序列是seq idno:10的第90-96位氨基酸(wss nppi)。
110、上述诊断中的抗体、多肽或抗原结合片段,为将35nidmab除cdr外其余位置氨基酸进行突变得到的抗体;或,所述抗体为将35nidmab进行人源化的抗体。
111、本领域技术人员可以根据本领域公知常识和惯用手段,将上述任一所述抗体,除了cdr序列之外的其它氨基酸进行改造突变,得到的抗体也属于本技术的保护范围。
112、所述人源化抗体为如下中至少一种:ae001-h1+l1、ae001-h2+l2或ae001-h3+l3。这三种抗体的均具有轻链可变区和重链可变区,重链可变区中含有cdr1,cdr2和cdr3,cdr1的序列是seq id no:9的第25-32位氨基酸(gytftnyg),cdr2的序列是seq id no:9的第50-57位氨基酸(intytge p),cdr3的序列是seq id no:9的第98-106位氨基酸(ygyswamdy);轻链可变区中含有cdr1,cdr2和cdr3,cdr1的序列是seq id no:10的第26-31位氨基酸(sssvsy),cdr2的序列是seq id no:10的第49-51位氨基酸(dts),cdr3的序列是seq idno:10的第90-96位氨基酸(wssnppi)。
113、ae001-h1+l1的重链恒定区序列为ae001h1(seq id no:1),轻链恒定区序列为ae001l1(seqid no:3)。
114、ae001-h2+l2的重链恒定区序列为ae001h2(seq id no:5),轻链恒定区序列为ae001l2(seqid no:7)。
115、ae001-h3+l3的重链恒定区序列为ae001h3(seq id no:11),轻链恒定区序列为ae001l3(se q id no:12)。
116、上述诊断中的抗体、多肽或抗原结合片段,所述抗体为将35nidmab或其人源化抗体中的至少一个cdr中氨基酸残基进行突变得到的抗体。
117、上述诊断中的抗体、多肽或抗原结合片段,所述将35nidmab或其人源化抗体中的至少一个cdr进行突变为进行如下至少一种突变:
118、35nidmab的重链可变区cdr1的第25、26、27、28、29和/或32位氨基酸残基进行突变;即(25gytftnyg 32)中除了ny其余氨基酸位置进行突变
119、35nidmab的重链可变区cdr2的第50、52、55、56和/或57位氨基酸残基进行突变;即(50int ytgep 57)中除了下划线氨基酸外其余位置的氨基酸进行突变
120、35nidmab的重链可变区cdr3的第98、99、101、103、104、105和/或106位氨基酸残基进行突变;即(98ygyswamdy 106)中除了下划线氨基酸外其余位置的氨基酸进行突变
121、35nidmab的轻链可变区cdr1的第26、27、28和/或29位氨基酸残基进行突变;即(26sssvsy 31)中除了下划线氨基酸外其余位置的氨基酸进行突变
122、35nidmab的轻链可变区cdr3的第90、91、94、95和/或96位氨基酸残基进行突变;即(90wssnppi 96)中除了下划线氨基酸外其余位置的氨基酸进行突变。
123、在35nidmab的抗体重链可变区cdr1序列(25gytftnyg 32)中,与抗原结合的主要是asn30和tyr31两个氨基酸;在抗体重链可变区cdr2序列(50intytgep 57)中,与抗原结合的主要是asn51,tyr53以及thr54三个氨基酸;在抗体重链可变区cdr3(98ygyswamdy 106)序列中,与抗原结合的主要是tyr100和trp102两个氨基酸。以上所述残基可以称为抗体重链与抗原相互作用残基。其它cdr残基不与或者很少与抗原ifp35结合,因此更易进行更改而获得不显著影响抗体活性的抗体。因此更改任何以上所述cdr中不与抗原相互作用的残基,仍然可能保持与ifp35或nmi的抗原-抗体复合体结构中对应的抗原表位氨基酸结合,应在本技术保护范围内。
124、在抗体轻链可变区cdr1序列(26sssvsy 31)中,与抗原结合的主要氨基酸是ser30和tyr31;在抗体轻链可变区cdr2序列(49dts 51)中,与抗原结合的主要氨基酸是asp49;在抗体轻链可变区cdr3序列(90wssnppi 96)中,与抗原结合的主要氨基酸是ser92和asn93。以上所述残基可以称为抗体重链与抗原相互作用残基。其它cdr残基不与或者很少与抗原ifp35结合,因此更易进行更改而获得不显著影响抗体活性的抗体。因此更改任何以上所述cdr中不与抗原相互作用的残基,仍然可能保持与ifp35或nmi的抗原-抗体复合体结构中对应的抗原表位氨基酸结合,应在本技术保护范围内。
125、上述诊断中的抗体、多肽或抗原结合片段,所述将35nidmab或其人源化抗体中的至少一个cdr进行突变为进行如下至少一种突变:
126、35nidmab的重链可变区cdr1的第30和/或31位氨基酸残基进行突变;
127、35nidmab的重链可变区cdr2的第51、53和/或54位氨基酸残基进行突变;
128、35nidmab的重链可变区cdr3的第100和/或102位氨基酸残基进行突变;
129、35nidmab的轻链可变区cdr1的第30和/或31位氨基酸残基进行突变;
130、35nidmab的轻链可变区cdr3的第92和/或93位氨基酸残基进行突变。
131、上述诊断中的抗体、多肽或抗原结合片段,所述抗体或抗原结合片段是能够识别如下两个或以上氨基酸残基的抗体或抗原结合片段:35nidmab或其人源化抗体中的重链的asn30、tyr31、asn51、tyr53、thr54、tyr100和trp102位氨基酸残基,其参与与抗原ifp35及nmi的识别。
132、上述诊断中的抗体、多肽或抗原结合片段,述抗体或抗原结合片段是能够识别如下两个或以上氨基酸残基的抗体或抗原结合片段:35nidmab或其人源化抗体中的轻链的ser30、tyr31、asp49、ser92和as n93位氨基酸残基,其参与与抗原ifp35及nmi的识别。
133、在抗体重链可变区cdr1序列(25gytftnyg 32)中,与抗原结合的主要是asn30和tyr31两个氨基酸;在抗体重链可变区cdr2序列(50intytgep 57)中,与抗原结合的主要是asn51,tyr53以及thr54三个氨基酸;在抗体重链可变区cdr3(98ygyswamdy 106)序列中,与抗原结合的主要是tyr100和trp102两个氨基酸。因此,改变其中部分氨基酸都可能有利于抗原抗体的结合能力。以上所述残基可以称为抗体重链与抗原相互作用残基。更改这些与抗原相互作用残基的任何1个或2个或3个,仍然保持与ifp35或nmi的抗原-抗体复合体结构中对应的抗原表位氨基酸结合,应在本技术保护范围内。
134、在抗体轻链可变区cdr1序列(26sssvsy 31)中,与抗原结合的主要氨基酸是ser30和tyr31;在抗体轻链可变区cdr2序列(49dts 51)中,与抗原结合的主要氨基酸是asp49;在抗体轻链可变区cdr3序列(90wssnppi 96)中,与抗原结合的主要氨基酸是ser92和asn93。因此,部分这些氨基酸的改变都可能有利于抗原抗体的结合能力。以上所述残基可以称为抗体轻链与抗原相互作用残基。更改这些与抗原相互作用残基的任何1个或2个或3个,仍然保持与ifp35或nmi的抗原-抗体复合体结构中对应的抗原表位氨基酸结合,应在本技术保护范围内。
135、上述诊断中的抗体、多肽或抗原结合片段,所述将35nidmab或其人源化抗体中的至少一个cdr进行突变得到的抗体为如下至少一种:
136、ae001-5、ae001-6、ae001-7、ae001-8、ae001-9的重链可变区的cdr和轻链可变区的cdr如下表所示。
137、重链可变区cdr:
138、
139、轻链可变区cdr:
140、
141、
142、ae001-5、ae001-6、ae001-7、ae001-8、ae001-9的重链可变区和轻链可变区除cdr以外的序列,本领域技术人员可以根据自己的需要进行改造。具体的一个例子,ae001-5、ae001-6、ae001-7、ae001-8、ae001-9的重链可变区和轻链可变区除cdr以外的序列,还可以与35nidmab抗体的相应序列相同相同。
143、ae001-5、ae001-6、ae001-7、ae001-8、ae001-9的恒定区序列,本领域技术人员可以根据自己的需要进行改造。具体的一个例子,ae001-5、ae001-6、ae001-7、ae001-8、ae001-9的恒定区序列可与上述ae001-h1+l1、ae001-h2+l2或ae001-h3+l3的恒定区序列相同。
144、上述诊断方法和应用中,所述慢性炎症疾病为与ifp35/nmi异常分泌到血液或体液中导致的炎症反应升高有关,包括关节炎、类风湿关节炎、银屑病(牛皮癣)、各种肠炎(如ibd)、多发性硬化症、哮喘、慢阻肺、系统性红斑狼疮、慢性肝炎、慢性肾炎、慢性胰腺炎、脑炎、恶性肿瘤、白血病、阿尔兹海默症、帕金森综合征、过敏性疾病、心血管疾病、肌肉骨骼疾病、炎性肠炎、肥胖及糖尿病、视网膜炎症疾病、牙周炎、葡萄膜炎等。
145、上述诊断方法和应用中,所述慢性炎症疾病为与ifp35/nmi异常分泌到血液或体液中导致的炎症反应升高有关,包括关节炎、类风湿关节炎、银屑病(牛皮癣)、各种肠炎(如ibd)、多发性硬化症、哮喘、慢阻肺、系统性红斑狼疮、慢性肝炎、慢性肾炎、慢性胰腺炎、脑炎、恶性肿瘤、白血病、阿尔兹海默症、帕金森综合征、过敏性疾病、炎性肠炎等。以上慢性炎症已被反复证明与多种炎症因子有关。
146、上述诊断方法和应用中,所述诊断为早期诊断、病情诊断和预后判断。
147、本技术还提供了ifp35的抗原表位。ifp35的抗原表位,为如下氨基酸残基中的至少一个:ifp35的arg163,asn164,arg191,gln194,ile195,gln197,phe198,thr199,pro201,gln206,pro208,arg210。
148、本技术还提供了nmi的抗原表位。nmi的抗原表位,为如下氨基酸残基中的至少一个:nmi的arg185,asn186 lys215,lys218,lys219,glu221,tyr222,pro223,tyr225,cys230,arg232,thr234。
149、本技术还提供了基于上述抗原表位制备抗体的方法。
150、本技术还提供的制备ifp35或nmi的抗体的方法,为利用上述任一述抗原表位信息制备得到ifp35或nmi的抗体。
151、上述制备ifp35或nmi的抗体的方法,为,基于以下35nidmab抗体-ifp35/nmi抗原复合体结构信息及序列信息进行抗体序列改造,然后制备得到改造的ifp35或nmi的抗体:
152、所述35nidmab抗体-ifp35/nmi抗原复合体结构信息如下:
153、在抗体35nidmab重链可变区cdr1序列(25gytftnyg 32)中,与抗原结合的主要是asn30和tyr31两个氨基酸;在抗体重链可变区cdr2序列(50intytgep 57)中,与抗原结合的主要是asn51,tyr53以及thr54三个氨基酸;在抗体重链可变区cdr3(98ygyswamdy 106)序列中,与抗原结合的主要是tyr100和trp102两个氨基酸。
154、在抗体35nidmab轻链可变区cdr1序列(26sssvsy 31)中,与抗原结合的主要氨基酸是ser30和tyr31;在抗体轻链可变区cdr2序列(49dts 51)中,与抗原结合的主要氨基酸是asp49;在抗体轻链可变区cdr3序列(90wssnppi 96)中,与抗原结合的主要氨基酸是ser92和asn93。
155、本领域技术人员公知,根据特定的抗原表位结构可以帮助设计、改造已有的原始抗体。原始抗体一般还是要通过各种筛选技术获得。知道了抗原表位(抗原决定簇)还可以直接用此片段筛选抗体。
156、以上所述抗体-抗原复合体结构信息及序列比对信息,(1)可以直观的看到位于抗原表面的氨基酸残基,由于抗原决定簇大多分布在抗原表面,所以这些表面残基可以帮助寻找抗原决定簇;(2)可以看到抗原与抗体相互作用的残基,从而可以分析抗原、抗体氨基酸残基之间相互作用特点,帮助针对特点的氨基酸残基进行改造、设计、及优化抗体。(3)可以指导改造抗体,从而获得针对其它同源蛋白抗原的新的抗体。
157、抗体基因改造方法涉及通用的基因定点突变技术及改造后的抗体基因或抗体基因片段(如抗体可变区)可以通过真核细胞(如哺乳动物细胞)或原核细胞进行表达、纯化,获得改造后的纯化的单克隆抗体。
158、由上述任一所述方法制备得到的抗体也属于本技术的保护范围。
159、本文所述的35nidmab抗体,具有轻链可变区和重链可变区,重链可变区中含有cdr1,cdr2和cdr3,cdr1的序列是seq id no:9的第25-32位氨基酸(gytftnyg),cdr2的序列是seq id no:9的第50-57位氨基酸(intytgep),cdr3的序列是seq id no:9的第98-106位氨基酸(ygyswamd y);轻链可变区中含有cdr1,cdr2和cdr3,cdr1的序列是seq id no:10的第26-31位氨基酸(ss svsy),cdr2的序列是seq id no:10的第49-51位氨基酸(dts),cdr3的序列是seq id no:10的第90-96位氨基酸(wssnppi)。
160、本文所述的35nidmab抗体,轻链可变区的序列是seq id no:10,重链可变区的序列是seq id no:9。
161、人源ifp35的氨基酸序列为seq id no:2。
162、鼠源ifp35的氨基酸序列为seq id no:4。
163、鼠源的nmi的氨基酸序列为seq id no:6。
164、人源的nmi的氨基酸序列为seq id no:8。
165、在此申请中,本技术发明人构建了一些炎症疾病的小鼠模型,并检测了这些炎症疾病动物血清中ifp 35及nmi含量,以此来寻找与ifp35/nmi相关的炎症疾病。本技术发明人发现的ifp35和nmi与一些慢性炎症疾病,如多发性硬化症密切相关,其血清含量高与多发性硬化症发病密切相关,ifp35/nmi基因敲除或使用针对ifp35/nmi的中和性抗体可以减轻多发性硬化症的症状。因此,本技术发明人认为抑制ifp 35或nmi活性可以用于治疗多发性硬化症等慢性疾病。检测血清或体液中(如脑脊液中)的ifp35和nmi含量可以用于慢性炎症疾病的诊断。
166、据此,本技术发明人开发了可以抑制ifp35的中和性抗体,为了更清楚的揭示抗体的抑制作用机制,本技术发明人进而解析了该中和性抗体与抗原ifp35的一个nid结构域的复合体三维晶体结构。通过这一复合体结构,本技术发明人可以揭示抗体的结构、抗原结构及抗体识别表位、抗原-抗体结合方式及关键相互作用残基等,并可以通过这一结构指导进行抗体的优化改造,以使其提高结合能力及增强识别的特异性,提高抗体的中和性活性。另外,由于ifp35与nmi序列上的高度同源性,还可以据此设计改造提高识别nmi蛋白能力的抗体,从而也开发出针对nmi的特异性抗体以及可以同时针对ifp35及nmi的双特异性抗体。
167、慢性炎症部分:本技术发明人检测了一些炎症疾病中是否存在ifp35或nmi表达提高的情况。本技术发明人发现,在多发性硬化(multiple sclerosis,ms)疾病小鼠模型中,nmi在血清中含量显著提高。基因敲除ifp35及nmi后,多发性硬化(multiple sclerosis)疾病小鼠的症状显著减轻。使用针对ifp35的中和性抗体可以缓解ms症状,达到治疗或改善疾病的目的。
168、在本技术的另外一部分内容中,本技术的发明人在研究流感病毒以及宿主免疫机制中,发现了人体中一种新型的damp类炎症因子ifp35家族蛋白(包含ifp35和nmi)。这类因子在正常人和鼠血清中很低或低于可检测水平(检测线以下水平);在病原感染情况下,能迅速从免疫细胞(巨噬细胞)中释放到血液中;能迅速促进免疫细胞分泌tnf、il6等炎症因子,激活机体的炎症反应;在血清中的含量与炎症反应程度正相关;在脓毒症病患样品进行检测时发现,当血液中ifp35和nmi含量达到较高水平(例如ifp达到数百pg/ml)时,病患死亡率较高。
169、本技术的发明人以流感病毒为模型,研究了此种炎症因子与病毒感染之间的关系后发现,与野生型小鼠相比,ifp35和/或nmi家族蛋白基因敲除的小鼠体重减轻状况大大缓解,临床症状显著减轻,流感病毒感染导致的肺损伤显著减轻,存活率显著提高。使用ifp35和/或nmi的中和性抗体治疗可以达到与基因敲除相当的效果,大大减轻患病小鼠的症状,显著降低流感病毒感染导致的死亡率。
170、基于上述研究成果,本技术的发明人探索此种炎症因子能够作为covid-19感染的血液检测标志物,用以帮助医护人员判断患者疾病严重程度及预后,并可以作为抑制过度炎症反应的靶标应用于病毒导致的过度炎症反应(或称脓毒症)的治疗,并由此建立了本技术的一项或多项发明。
171、研究结果表明:感染新型冠状病毒covid-19的重症/危重症患者的血清中ifp35和nmi的水平显著提高,表明ifp35和nmi可以作为重症/危重症患者的诊断或辅助诊断指标,从而为帮助医护人员提供警示。此外,结合以ifp35和nmi作为靶标的流感病毒研究结果,针对ifp35和nmi的抑制剂药物(例如抗体药物)有望用于covid-19导致的过度炎症反应疾病的治疗。无论是流感病毒或是新型冠状病毒co vid-19,在感染人体后都会引起ifp35及nmi分泌到血液及体液中。当敲除这两种炎症因子ifp35和nmi中的任一基因或使用中和抗体对其中一个基因进行抑制后,感染的机体炎症反应降低,死亡率下降,这些结果说明分泌的ifp35和nmi与病毒(以流感病毒和新型冠状病毒covid-19为例)的感染严重程度相关,可以作为这些病毒导致的机体炎症反应的指标,并且可以成为抗体药物、多肽药物或化学药物等抑制剂的治疗靶标。
172、定义
173、除非另有定义,否则本文使用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常理解的相同的含义。本文引用的所有专利、专利申请(公开的或未公开的)和其它出版物的通过引用以其整体并入本文。如果本部分中阐述的定义与通过引用并入本文的专利、申请、公开的申请和其它出版物中阐述的定义相反或不一致,则以本部分中阐述的定义为准。
174、本文中的病毒包括能够引发被感染的机体中炎症反应、特别是过度/重度炎症反应(炎症因子风暴)的病毒,包括但不限于冠状病毒科(例如冠状病毒,包括covid-19、sars、mers病毒)、正粘病毒科(例如,流感病毒,例如甲型(a型)流感病毒)、负链rna病毒目的其它病毒(如埃博拉病毒、拉沙病毒、马尔堡病毒、克里米亚-刚果出血热病毒)、逆转录病毒科(例如人免疫缺陷病毒,例如hiv-1(也称为htlv-iii、lav或htlv-iii/lav或hiv-iii);以及其他分离株,例如hiv-lp、小核糖核酸病毒科(例如脊髓灰质炎病毒、甲型肝炎病毒、肠道病毒、人柯萨奇病毒、鼻病毒、回声病毒)、calciviridae(例如引起肠胃炎的菌株)、披膜病毒科(例如马脑炎病毒、风疹病毒)、黄病毒科病毒,如寨卡病毒、西尼罗病毒、登革热病毒、汉坦病毒等)、弹状病毒科(例如水泡性口炎病毒、狂犬病毒)、丝状病毒科(例如埃博拉病毒)、副粘病毒科(例如副流感病毒、腮腺炎病毒、麻疹病毒、呼吸道合胞病毒)、双链rna病毒科(例如bunga病毒、静脉炎病毒和nairo病毒)、肾炎病毒科(出血热病毒)、呼肠孤病毒科轮状病毒)、双抗病毒科肝炎病毒科(乙型肝炎病毒)、细小病毒科(细小病毒)、乳头状病毒科(乳头瘤病毒、多瘤病毒)、腺病毒科(大多数腺病毒)、疱疹病毒科(单纯疱疹病毒(hsv)1和2、水痘带状疱疹病毒、巨细胞病毒(cmv)、疱疹病毒)、痘病毒(天花病毒、牛痘病毒、痘病毒)和虹彩病毒(例如,非洲猪瘟病毒)、丙型肝炎病毒和未分类的病毒(例如,δ型肝炎(被认为是乙型肝炎病毒的有缺陷的卫星)、诺瓦克和相关病毒,和星状病毒)。
175、本文中的“生物样品”是指感染病毒的个体中获取的含有细胞分泌物的样品,包括但不限于血液、血浆、血清、脑脊液、肺泡灌洗液、尿液、汗液、粪便等。
176、本文中的“个体”不限于特定物种或样品类型。例如,术语“个体”可以指患者,并且通常是人类患者。然而,该术语不限于人,因此包括多种非人动物或哺乳动物物种。“哺乳动物”是指任何哺乳动物种类的物种。通常,本文所用的术“哺乳动物”是指人、人类受试者或人类患者。“哺乳动物”还指任何非人哺乳动物种类的物种,例如实验、伴侣或经济性的非人哺乳动物。示例性非人哺乳动物包括小鼠、大鼠、兔、猫、狗、猪、牛、绵羊、山羊、马、猴、大猩猩和黑猩猩。
177、本文中的“治疗有效量”或“有效量”是指当单独或与其它治疗剂组合施用于细胞、组织或受试者时有效的治疗剂的量预防或改善受试者中与异常高水平的ifp35和/或nmi相关的疾病或不适。治疗有效剂量还指治疗剂的量足以导致症状的改善,例如治疗、治愈、预防或缓解相关医学不适,或提高治疗、治愈、预防或缓解这种病况的速度。当应用于单独施用的单个活性成分时,治疗有效剂量是指单个的该成分。当应用于组合时,治疗有效剂量是指导致治疗效果的活性成分的组合量,无论是组合、连续或同时施用。在一些实施方案中,“治疗特定疾病的化合物的有效量”是足以缓解或以某种方式减少与疾病相关的症状的量。这样的量可以作为单一剂量施用或可以根据方案施用,从而其是有效的。所述量可治愈疾病,但通常是为了改善疾病的症状而施用。可能需要重复给药以实现期望的症状缓解。
178、本文中的术语“药学上可接受的载体”指在包括与药物施用相容的任何和所有溶剂、分散介质、包衣、等渗剂和吸收延迟剂等。这些介质和试剂用于药物活性物质的用途是本领域熟知的。见,例如remington,the science and practice of pharmacy,第20版,(lippincott,williams&wilkins 2003)。除非任何常规介质或试剂与活性化合物不相容,否则考虑在组合物中的这种用途。
179、本文所用的术语“抑制剂”指能对ifp35和/或nmi的生物学作用产生负性影响的任何分子,例如,可通过干扰ifp35和/或nmi与另一分子(例如,其底物)的相互作用,或降低ifp35和/或nmi的蛋白水平,例如通过降低编码ifp35和/或nmi的基因的表达。抑制剂可为“直接的抑制剂,”其与ifp35和/或nmi或编码ifp35和/或nmi的核酸相互作用,或者“间接的抑制剂,”其不与ifp35和/或nmi或编码ifp35和/或nmi的核酸相互作用,但与调控通路中ifp35和/或nmi的上游或下游相互作用。抑制剂可以为特异性抑制剂。本领域技术人员能够理解,虽然利用特异性抑制剂是比较理想的,但是根据具体情况,使用多功能或通用型蛋白抑制剂也是可选的。如上文所讨论的,抑制剂可以为表达抑制剂、功能抑制剂、或同时能抑制表达和功能的抑制剂。在一些实施方案中,抑制剂为能作用于ifp35和/或nmi的转录和/或翻译水平从而降低生成的功能性ifp35和/或nmi的量的抑制剂。在一些相关实施方案中,抑制剂包括,但不限于,dsrna、microrna、sirna、shrna、反义rna或核酶。利用rna干扰/沉默技术、反义核酸技术或核酶技术降低目标蛋白的表达水平是本领域技术人员所公知的,并且根据目标蛋白(例如,ifp35和/或nmi)的序列结构设计出合适的dsrna、microrna、sirna、shrna、反义rna或核酶分子以及相应的制备和测试检验也是本领域技术人员容易实现的。在一些实施方案中,抑制剂为能抑制ifp35和/或nmi功能/活性的抑制剂。在一些相关实施方案中,抑制剂包括但不限于,针对ifp35和/或nmi的抗体或其抗原结合片段、小分子化合物。可用于本技术的抗体可包括多克隆抗体或单克隆抗体。此外,抗体可为来源于天然来源或来自重组来源的整个免疫球蛋白。抗体可以各种形式存在,包括例如作为整个抗体,或作为抗体片段,或它们的其他免疫活性片段如互补决定区。类似地,抗体可作为具有功能性抗原结合结构域,即重链和轻链可变域的抗体片段存在。同样,抗体片段可以选自但不限于如下的形式存在:fv、fab、f(ab)2、scfv(单链fv)、dab(单结构域抗体)、双特异性抗体、双链抗体和三链抗体。
180、另一方面,本技术提供了诊断或评估感染病毒的个体的炎症反应程度的方法,包括测定获自所述个体的生物样品中干扰素诱导蛋白35kd(ifp35)和/或n-myc相互作用蛋白(nmi)的量。
181、在一些实施方案中,所述方法用于诊断或辅助诊断重症或危重症患病个体。
182、在一些实施方案中,所述病毒为冠状病毒科的病毒,例如新型冠状病毒(covid-19)、sars病毒、mers病毒;或正粘病毒科的病毒,例如流感病毒(甲型流感病毒)。
183、在一些实施方案中,测定生物样品中ifp35和/或nmi的量为测定生物样品中ifp35和/或nmi的蛋白含量,或测定生物样品中ifp35和/或nmi的核酸水平表达量,例如mrna含量。
184、在一些实施方案中,个体为哺乳动物,例如人类。
185、在一些实施方案中,生物样品为血液、血浆、血清、脑脊液或肺泡灌洗液。
186、另一方面,本技术提供了用于诊断或评估感染病毒的个体的炎症反应程度的试剂盒,包括用于测定获自所述个体的生物样品中干扰素诱导蛋白35kd(ifp35)和/或n-myc相互作用蛋白(nmi)的量的试剂。
187、在一些实施方案中,试剂盒用于诊断或辅助诊断重症或危重症患病个体。
188、在一些实施方案中,所述病毒为冠状病毒科的病毒,例如新型冠状病毒(covid-19)、sars病毒、mers病毒;或正粘病毒科的病毒,例如流感病毒(甲型流感病毒)。
189、在一些实施方案中,测定生物样品中ifp35和/或nmi的量为测定生物样品中ifp35和/或nmi的蛋白含量,例如所述试剂包括特异性结合ifp35和/或nmi的抗体。
190、在一些实施方案中,测定生物样品中ifp35和/或nmi的量为测定生物样品中ifp35和/或nmi的核酸水平表达量,例如mrna含量,例如所述试剂包括针对ifp35和/或nmi的cdna序列设计的特异性扩增引物。
191、在一些实施方案中,个体为哺乳动物,例如人类。
192、在一些实施方案中,所述试剂包括用于处理所述生物样品以提取蛋白或核酸物质的试剂,例如,所述生物样品为血液、血浆、血清、脑脊液或肺泡灌洗液。
193、另一方面,本技术提供了治疗或缓解感染病毒的个体的炎症反应的方法,包括给予所述个体治疗有效量的干扰素诱导蛋白35kd(ifp35)和/或n-myc相互作用蛋白(nmi)的抑制剂。
194、在一些实施方案中,所述个体为重症或危重症患病个体。
195、在一些实施方案中,所述病毒为冠状病毒科的病毒,例如新型冠状病毒(covid-19)、sars病毒、mers病毒;或正粘病毒科的病毒,例如流感病毒(甲型流感病毒)。
196、在一些实施方案中,所述ifp35和/或nmi的抑制剂为ifp35和/或nmi的功能抑制剂或表达抑制剂。
197、在一些实施方案中,所述ifp35和/或nmi的功能抑制剂为ifp35和/或nmi的抗体或其抗原结合片段,或小分子化合物。
198、在一些实施方案中,所述ifp35和/或nmi的表达抑制剂为能作用于ifp35和/或nmi的转录和/或翻译水平从而降低生成的功能性ifp35和/或nmi的量的抑制剂,例如dsrna、microrna、sirn a、shrna、反义rna或核酶。
199、在一些实施方案中,所述个体为哺乳动物,例如人类。
200、另一方面,本技术提供了用于治疗或缓解感染病毒的个体的炎症反应的药物组合物,包括治疗有效量的干扰素诱导蛋白35kd(ifp35)和/或n-myc相互作用蛋白(nmi)的抑制剂,以及药学上可接受的载体。
201、在一些实施方案中,所述个体为重症或危重症患病个体。
202、在一些实施方案中,所述病毒为冠状病毒科的病毒,例如新型冠状病毒(covid-19)、sars病毒、mers病毒;或正粘病毒科的病毒,例如流感病毒(甲型流感病毒)。
203、在一些实施方案中,所述ifp35和/或nmi的抑制剂为ifp35和/或nmi的功能抑制剂或表达抑制剂。
204、在一些实施方案中,所述ifp35和/或nmi的功能抑制剂为ifp35和/或nmi的抗体或其抗原结合片段,或小分子化合物。
205、在一些实施方案中,所述ifp35和/或nmi的表达抑制剂为能作用于ifp35和/或nmi的转录和/或翻译水平从而降低生成的功能性ifp35和/或nmi的量的抑制剂,例如dsrna、microrna、sirn a、shrna、反义rna或核酶。
206、在一些实施方案中,所述个体为哺乳动物,例如人类。
207、应当理解,以上详细描述仅为了使本领域技术人员更清楚地了解本技术的内容,而并非意图在任何方面加以限制。本领域技术人员能够对所述实施方案进行各种改动和变化。
本文地址:https://www.jishuxx.com/zhuanli/20241021/318219.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。