靶向ACSL4基因的反义寡核苷酸及其应用
- 国知局
- 2024-09-19 14:37:57
本发明属于生物与生物制药,具体地说是靶向acsl4基因的反义寡核苷酸及其应用。
背景技术:
1、脑卒中也称为中风,是一种急性脑血管疾病。是指由于大脑血管缺血或者出血导致脑部血流供应中断最终引起脑组织损伤的一种疾病,其中缺血性脑卒中(ischemicstroke,is)约占脑卒中总数的85%。目前抗is的药物研究主要涉及溶栓和神经保护。临床研究显示在缺血发生后的4.5h内溶解血栓以恢复血流灌注,可挽救濒临死亡的脑神经细胞,4.5-6h后使用则由于缺血再灌注损伤导致病理损伤加重,死亡率升高。因此,溶栓药物的使用有严格的时间窗限制。神经保护曾被认为是is治疗的希望,但至今仍没有一个独立的神经保护剂得到临床疗效的支持。因此,寻找有效的治疗策略及药物极为重要。
2、近年来研究发现,铁死亡途径在缺血性脑卒中的损伤过程中介导着神经细胞的死亡。铁死亡是2012年发现的一种新的细胞死亡模式。主要是由脂质过氧化物在细胞膜上的毒性积聚引发的,通过抑制抗氧化防御系统和铁依赖性活性氧(ros)的积累,与多不饱和脂肪酸(pufas)反应并破坏细胞膜的完整性。铁死亡的标志性特点就是细胞质膜中多不饱和脂肪酸(pufa)的过氧化积累。铁死亡是脑缺血-再灌注损伤中最重要的细胞死亡方式之一,已被证明参与脑缺血再灌注过程。因此,is后的铁死亡是对抗is潜在的治疗靶点。
3、acsl4基因全称为长链脂肪酰辅酶a合酶4(acyl-coasynthetaselong-chainfamilymember4),这个基因编码一种酶,用于催化长链脂肪酸和辅酶a(coa)结合形成长链脂肪酰-coa。长链脂肪酰-coa是脂质代谢和生物膜合成的关键中间体。acsl4通过催化生成脂肪酰-coa,增加了细胞膜pufas的含量,进而增加细胞对铁死亡的敏感性。此外,acsl4表达水平可能影响细胞内抗氧化防御系统的活性,包括抗氧化物质如谷胱甘肽(gsh)和相关的酶系统。当抗氧化防御系统受到抑制时,膜中的pufa过氧化会无法得到有效抑制,从而加剧铁死亡。因此,acsl4的表达和活性与铁死亡的敏感性密切相关。高表达或活性的acsl4会增加细胞对铁死亡的易感性,而抑制acsl4的表达或活性则可以保护细胞免受铁死亡的影响。鉴于此,开发acsl4的抑制性药物,对预防缺血性脑卒中的神经损伤具有十分重要的意义。
4、为此,本领域技术人员提出了靶向acsl4基因的反义寡核苷酸及其应用来解决背景技术提出的问题。
技术实现思路
1、为了解决上述技术问题,本发明提供靶向acsl4基因的反义寡核苷酸及其应用,目的是提供一种毒性低、特异性好的acsl4蛋白表达抑制剂。
2、本发明的另一目的是提供一种用于预防脑卒中过程中神经死亡的药物。
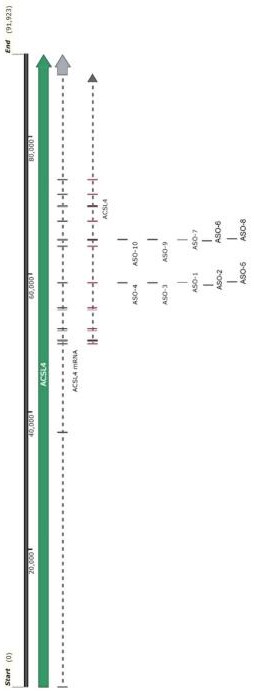
3、为达到上述目的,本发明提供靶向acsl4基因的反义寡核苷酸药物,其操作步骤如下:与acsl4 mrna序列特异性结合,通过与acsl4 mrna形成dna-rna杂交链,利用内源rnaseh1对rna进行切割,从而导致acsl4 mrna及蛋白水平的降低;本发明提供的acsl4的反义寡核苷酸包含如下所示:aso-1、aso-2、aso-3、aso-4、aso-5、aso-6、aso-7、aso-8、aso-9、aso-10;
4、其中,aso-1的序列如seq id no.1所示:5’-tgtactcaccggaacagcag-3’;
5、aso-2的序列如seq id no.2所示:5’-gtactcaccggaacagcagc-3’;
6、aso-3的序列如seq id no.3所示:5’-tgggcttcagtacagtacag-3’;
7、aso-4的序列如seq id no.4所示:5’-ttcagtacagtacagtctcc-3’;
8、aso-5的序列如seq id no.5所示:5’-tactcaccggaacagcagcc-3’;
9、aso-6的序列如seq id no.6所示:5’-tcccagcaccacatgattct-3’;
10、aso-7的序列如seq id no.7所示:5’-gcagacattcatgaatcggt-3’;
11、aso-8的序列如seq id no.8所示:5’-ccagcaccacatgattctgt-3’;
12、aso-9的序列如seq id no.9所示:5’-cagacattcatgaatcggtg-3’;
13、aso-10的序列如seq id no.10所示:5’-cattcatgaatcggtgtgtc-3’。
14、优选的,所述反义寡核苷酸的序列全链硫代磷酸修饰(ps,*所示),并在首尾两端各5个碱基的核糖引入2’-o-甲氧乙基修饰(2’-moe),胞嘧啶均为甲基胞嘧啶修饰,所述序列为seq id no.1-seq id no.10任意一种或者其任意组合,如下表:
15、
16、优选的,所述基因片段为序列seq id no.3、seq id no.7;
17、所述seq id no.3序列及修饰如下所示:
18、(moe-t)*(moe-g)*(moe-g)*(moe-g)*(moe-5-me-c)*(dt)*(dt)*(m5dc)*(da)*(dg)*(dt)*(da)*(m5dc)*(da)*(dg)*(moe-t)*(moe-a)*(moe-5-me-c)*(moe-a)*(moe-g);
19、所述seq id no.7序列如下所示:
20、(moe-g)*(moe-5-me-c)*(moe-a)*(moe-g)*(moe-a)*(m5dc)*(da)*(dt)*(dt)*(m5dc)*(da)*(dt)*(dg)*(da)*(da)*(moe-t)*(moe-5-me-c)*(moe-g)*(moe-g)*(moe-t);
21、反义寡核苷酸(antisense oligonucleotides,asos)是一种人工合成的经过化学修饰的单链寡核苷酸,他们的序列可以与靶目标rna碱基互补配对结合;aso与rna结合后会以多种方式影响rna的活性,最常见的作用机制是与靶rna结合后,诱导内源的rnase h1特异性切割目标rna,释放后的aso可继续作用于其他目标rna,从而起到抑制靶基因的目的;为了提高aso在体内的稳定性,还需要进行化学结构改造从而防止在体内被快速的降解;aso药物具有特异性高、作用方式多样、广泛的适用性、免疫原性低、毒性及不良反应小、研发周期短等优点,已成为各种疾病治疗的优选手段。
22、优选的,所述反义寡核苷酸的序列全链硫代磷酸修饰(ps,*所示),并在首尾两端各5个碱基的核糖引入2’-o-甲氧乙基修饰(2’-moe),胞嘧啶均为甲基胞嘧啶修饰。
23、优选的,所述反义寡核苷酸序列进行其他修饰,所述修饰类型包含lna、三环dna、2’-o甲基、2’环乙基(cet)、una、2’氟和构象受限的核苷。
24、本发明根据预测的acsl4的rna结构设计了10条靶向acsl4全长的反义寡核苷酸,本发明所提供的反义寡核苷酸序列的特异性和抑制acsl4的作用明显。
25、本发明所述含修饰的acsl4反义寡核苷酸主要包含在上述靶向acsl4的原始反义寡核苷酸序列上,添加一些特殊的化学修饰等,使这些序列更加稳定和适用于细胞转染实验和商品化应用;本发明所述10条反义寡核苷酸序列进行的化学修饰主要包括如下所述几种具体修饰类型:
26、本发明所述硫代磷酸酯键修饰指aso分子的每个核苷酸将磷酸二酯键(po)中的一个氧原子替换为硫原子(ps),这种修饰增强了aso对核酸酶的稳定性,并增强了aso与蛋白质结合的亲和力。
27、本发明所述2’-o-甲氧基乙基基团修饰指aso分子中5’-端和3’-端的5个连续核苷酸包含修饰的2’-o-甲氧基乙基(moe)基团;2’-o-甲氧基乙基基团是指呋喃糖基环的2’位的3甲氧基修饰(羟基修饰为甲氧乙基),2’-o-甲氧基乙基基团修饰可以增强核酸酶抵抗能力,减少脱靶效应并增强反义寡核苷酸的杂交亲和力。
28、本发明所述5-甲基脱氧核糖胞苷(5-me-dc)修饰指在胞嘧啶脱氧核糖核苷酸碱基的第五位修饰甲基;5-me-dc与dg碱基互补配对,该修饰提高了双链的稳定性并可以大幅减弱免疫反应;
29、本发明提供了在细胞中转染aso后q-pcr以及western blot的结果表明,aso-3,aso-7可以有效的敲低acsl4蛋白的表达,aso-7敲低效果更好,200nm可以敲低80%以上;本发明还提供了动物模型实验结果,表明在大鼠大脑中敲低acsl4后可以减少缺血再灌注损伤大鼠脑梗死面积。
30、与现有技术相比,本发明具有如下有益效果:
31、本发明提供的细胞实验以及动物模型实验证明acsl4反义寡核苷酸可以有效的缓解脑卒过程中对神经细胞的损伤,同时本发明的反义寡核苷酸作为一种新型核酸药物,可以用于脑卒中的辅助治疗,具有广阔的应用前景。
本文地址:https://www.jishuxx.com/zhuanli/20240919/299261.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。