确定高糖微环境下抑制细胞迁移的趋化因子及机制的方法与流程
- 国知局
- 2024-08-05 11:38:50
本发明涉及生物医药,尤其涉及一种确定高糖微环境下抑制细胞迁移的趋化因子及机制的方法。
背景技术:
1、据国际糖尿病联盟统计,全球有约5亿人患糖尿病,预计到2045年,该数字将达到7亿多人(占全球人口的7.8%)。糖尿病足是糖尿病最严重并发症中的一种,在高收入国家糖尿病足的年发病率为2%~4%,低收入国家糖尿病足的终身患病率为19%~34%。糖尿病足是非创伤性下肢截肢的主要原因。据报道,全世界每年因dfu导致不同程度截肢的人群超过100万。
2、当前常规治疗糖尿病足的方法主要包括:1).通过使用胰岛素、口服降糖药物或生活方式的调整来控制血糖水平,以减少糖尿病足的发病风险;2).使用抗血小板药物(如阿司匹林)、抗生素预防感染、改善血液循环的药物(如前列地尔)等;3).使用伤口敷料、清创、负压封闭引流(vac)等方法来促进创面愈合;4).在必要时进行手术治疗,包括截肢、血管重建、神经修复等。
3、通过对国内外相关专利文献的调研后发现,当前治疗方法仍存在以下难题尚未解决:1).常规西医治疗糖尿病足的疗效仅为70%,且对于严重或难愈合的创面效果不佳;2).依赖医生或护理人员的主观判断,缺乏客观的监测指标;3).难以适应多变的环境条件和个体差异,特别是在极端气候条件下;4).一些治疗方法(如截肢)成本较高,且术后恢复期长;
技术实现思路
1、针对现有技术的以上缺陷或改进需求,本发明的目的在于提供一种确定高糖微环境下抑制细胞迁移的趋化因子及机制的方法,这种方法通过单细胞测序和多种实验技术,旨在揭示高糖环境下趋化因子对细胞迁移的抑制作用及其分子机制。通过对比不同条件下细胞的迁移能力和相关蛋白的表达,确定高糖环境如何影响细胞行为,以及cxcl12等趋化因子在其中的作用,这种研究有助于理解高糖环境下细胞行为的调控机制,为相关疾病的预防和治疗提供理论基础。
2、第一方面,本发明提供一种确定高糖微环境下抑制细胞迁移的趋化因子及机制的方法,包括:
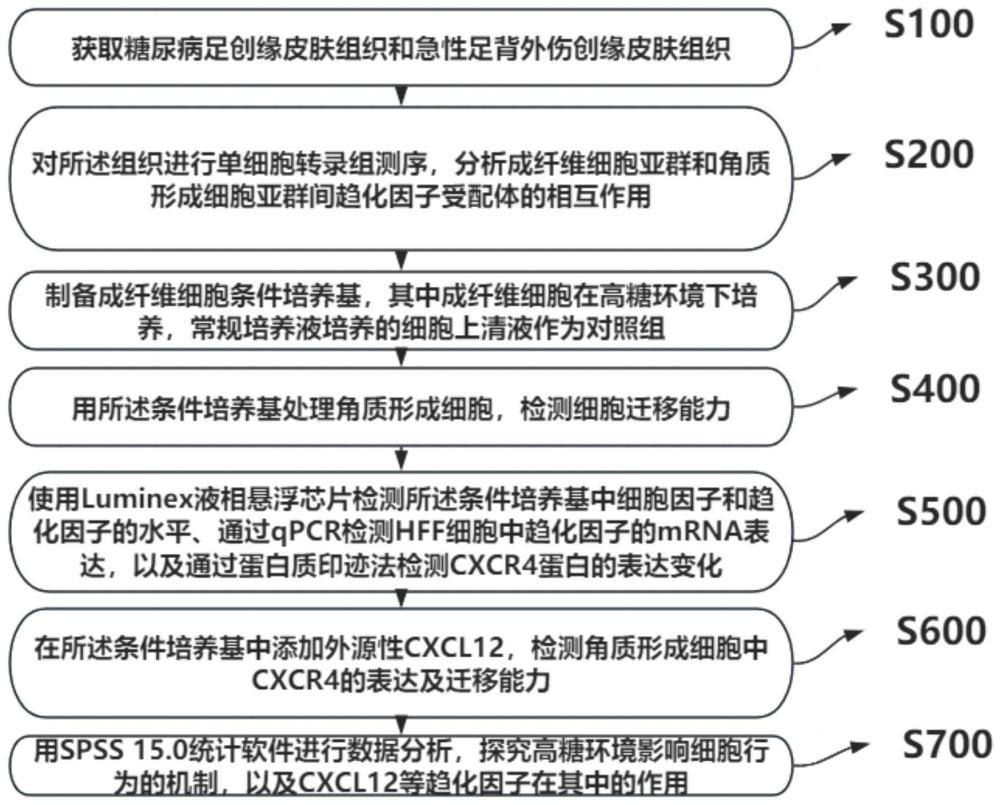
3、s100、获取糖尿病足创缘皮肤组织和急性足背外伤创缘皮肤组织;
4、s200、对所述组织进行单细胞转录组测序,分析成纤维细胞亚群和角质形成细胞亚群间趋化因子受配体的相互作用;
5、s300、制备成纤维细胞条件培养基,其中成纤维细胞在高糖环境下培养,常规培养液培养的细胞上清液作为对照组;
6、s400、用所述条件培养基处理角质形成细胞,检测细胞迁移能力;
7、s500、使用luminex液相悬浮芯片检测所述条件培养基中细胞因子和趋化因子的水平、通过qpcr检测hff细胞中趋化因子的mrna表达,以及通过蛋白质印迹法检测cxcr4蛋白的表达变化;
8、s600、在所述条件培养基中添加外源性cxcl12,检测角质形成细胞中cxcr4的表达及迁移能力;
9、s700、采用spss15.0统计软件进行数据分析,确定高糖环境影响细胞行为的机制,以及cxcl12等趋化因子在其中的作用。
10、进一步地,所述步骤s200具体包括:
11、取2型糖尿病足患者创缘皮肤和足外伤患者足背部创缘皮肤,进行分离、制备、文库构建以及单细胞转录组测序,并使用r包中的“cluster profiler”包进行go和kegg富集分析;使用cellphone db分析细胞间的相互作用;使用circlize v0.4.10 r软件包对结果进行可视化展示。
12、进一步地,所述细胞迁移能力通过划痕实验进行检测,包括:
13、用200ul的移液器枪头尖端刮擦单层细胞并用pbs清洗,每孔加入2ml培养液,划痕后0、24、48、72h在200倍光学显微镜下观察细胞划痕愈合情况并计算划痕后24、48、72h细胞迁移率。
14、进一步地,所述s400中所述划痕实验需重复三次,结果取其均值。
15、第二方面,本发明提供一种cxcl12/cxcr4信号通路作为靶点在制备治疗或预防糖尿病足的药物中的应用。
16、第三方面,本发明提供一种cxcl12/cxcr4信号通路激动剂在制备治疗糖尿病足的药物中的应用,所述信号通路激动剂包括cxcl12激动剂或cxcr4激动剂中的一种或多种。
17、进一步地,所述cxcl12激动剂包括激动cxcl12活性的物质或提高cxcl12水平的物质,所述cxcr4激动剂选自激动cxcr4活性的物质或提高cxcr4水平的物质。
18、进一步地,所述药物的剂型选自药学上允许的任意一种剂型;
19、进一步地,所述剂型选自片剂,颗粒剂,胶囊剂,丸剂,口服液,注射液,脂质体中的一种或多种;
20、进一步地,所述药物或药物组合物的给药方式选自口服给药,局部给药,鼻内给药,全身给药,静脉内给药,皮下给药,肌肉内给药,脑室内给药,鞘内给药或透皮给药中的一种或多种。
21、本发明的有益效果:
22、1.本发明的目的在于提供一种确定高糖微环境下抑制细胞迁移的趋化因子及机制的方法,这种方法通过单细胞测序和多种实验技术,旨在揭示高糖环境下趋化因子对细胞迁移的抑制作用及其分子机制。通过对比不同条件下细胞的迁移能力和相关蛋白的表达,确定高糖环境如何影响细胞行为,以及cxcl12等趋化因子在其中的作用,这种研究有助于理解高糖环境下细胞行为的调控机制,为相关疾病的预防和治疗提供理论基础。
23、2.本发明确定了高糖环境下成纤维细胞分泌的cxcl12蛋白减少是阻碍角质形成细胞迁移的重要因素之一,为糖尿病足的治疗提供了新的靶点。
24、3.本发明提出了一种利用cxcl12/cxcr4信号通路的激动剂作为治疗糖尿病足的药物,为糖尿病足的治疗提供了新的治疗策略。
25、本申请附加的方面和优点将在下面的描述中部分给出,这些将从下面的描述中变得明显,或通过本申请的实践了解到。
技术特征:1.一种确定高糖微环境下抑制细胞迁移的趋化因子及机制的方法,其特征在于,包括:
2.根据权利要求1所述的一种确定高糖微环境下抑制细胞迁移的趋化因子及机制的方法,其特征在于,所述步骤s200具体包括:
3.根据权利要求1所述的一种确定高糖微环境下抑制细胞迁移的趋化因子及机制的方法,其特征在于,所述步骤s400包括:
4.根据权利要求1所述的一种确定高糖微环境下抑制细胞迁移的趋化因子及机制的方法,其特征在于,所述步骤s400中划痕实验需重复三次,结果取其均值。
5.一种cxcl12/cxcr4信号通路作为靶点在制备治疗糖尿病足的药物中的应用。
6.一种cxcl12/cxcr4信号通路激动剂在制备治疗糖尿病足的药物中的应用,其特征在于,所述信号通路激动剂包括cxcl12激动剂或cxcr4激动剂中的一种或多种。
7.根据权利要求6所述的一种cxcl12/cxcr4信号通路激动剂在制备治疗糖尿病足的药物中的应用,其特征在于,所述cxcl12激动剂包括激动cxcl12活性的物质或提高cxcl12水平的物质,所述cxcr4激动剂选自激动cxcr4活性的物质或提高cxcr4水平的物质。
8.如权利要求5-7中任一项所述的一种cxcl12/cxcr4信号通路激动剂在制备治疗糖尿病足的药物中的应用,其特征在于,所述药物的剂型选自药学上允许的任意一种剂型。
9.如权利要求8所述的一种cxcl12/cxcr4信号通路激动剂在制备治疗糖尿病足的药物中的应用,其特征在于,所述剂型选自片剂,颗粒剂,胶囊剂,丸剂,口服液,注射液,脂质体中的一种或多种。
10.如权利要求8所述的一种cxcl12/cxcr4信号通路激动剂在制备治疗糖尿病足的药物中的应用,其特征在于,所述药物或药物组合物的给药方式选自口服给药,局部给药,鼻内给药,全身给药,静脉内给药,皮下给药,肌肉内给药,脑室内给药,鞘内给药或透皮给药中的一种或多种。
技术总结本发明公开了一种确定高糖微环境下抑制细胞迁移的趋化因子及机制的方法,包括:获取糖尿病足创缘皮肤组织或急性足背外伤创缘皮肤组织;对所述组织进行单细胞转录组测序,分析成纤维细胞亚群和角质形成细胞亚群间的趋化因子受配体相互作用;制备成纤维细胞条件培养基;用所述条件培养基处理角质形成细胞,检测细胞迁移能力;检测所述条件培养基中趋化因子CXCL12的表达水平;在所述条件培养基中添加外源性CXCL12,检测角质形成细胞中CXCR4的表达及迁移能力。结果表明,高糖环境可通过下调趋化因子及其受体的表达来抑制细胞迁移,从而影响组织修复和疾病进程。本方法有助于理解高糖环境下细胞行为的调控机制,为相关疾病的预防和治疗提供理论基础。技术研发人员:阮琼芳,章思语,阮晶晶受保护的技术使用者:武汉市第三医院技术研发日:技术公布日:2024/8/1本文地址:https://www.jishuxx.com/zhuanli/20240802/258594.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表