靶向组织因子的纳米抗体及偶联物的制备方法和用途
- 国知局
- 2024-10-21 14:24:00
本发明涉及医药领域,尤其涉及靶向组织因子的纳米抗体及纳米抗体-药物偶联物、其制备方法和用途。
背景技术:
1、组织因子(tissue factor,tf)是分子量47kd的跨膜糖蛋白。在生理状态下,当血管受到创伤后tf激活外源性凝血反应。然而tf在许多肿瘤组织中异常激活表达,其中,乳腺癌、胰腺癌、肺癌、食道癌等中都有很高的异常表达率,如在乳腺癌中tf异常表达率为85.8%,在胰腺癌中为88.5%,在肺癌中为83.6%,食道癌中为91.3%等((blood,2012,119:924-932)。tf/fviia复合物还能直接结合和诱导跨膜g蛋白偶联受体protease-activated receptor 2(par2)的活化。tf通过par2能影响细胞内一系列肿瘤功能信号,比如tf-par2通过mapk/erk磷酸化,诱导关键生长因子、免疫调节因子和趋化因子的基因表达,促进新生血管的形成,为肿瘤的生长提供了充足的养分、能量和适宜的微环境。此外,tf还可以通过与rac1、β1家族相关整合素的相互作用,以提高肿瘤细胞的迁移性和粘附性,从而在整体上增强肿瘤细胞的血行性转移能力(journal of thrombosis research,2012,130:s84-s87;journal of thrombosis and haemostasis,2013,11:285-293;international journal of cancer,2014,doi:10.1002/ijc.28959;blood,2012,119:924-932)。因此,鉴于当前国际上对tf相关疾病中的作用和功能的研究,开发靶向tf的特异性治疗抗体,对tf在癌症、血栓、炎症等各类疾病中引起的血管增生、异常凝血等所导致的病理特征的诊断、治疗和预防是极其有益的。全球首款靶向tf的抗肿瘤药物tivdak(tf-adctisotumab vedotin)已于2021年获批上市,数款不同制药企业开发的tf-adc处于临床研究阶段。
2、单克隆抗体药物已经为癌症治疗带来了突破,为多个癌症领域的临床治疗带来了改善。然而,传统单抗的分子量为150kd,使其实体瘤的穿透性和药物分布受限,治疗效果还有待进一步提高。纳米抗体(nanobody,nb)是羊驼自然产生的仅由重链组成的抗体,其中,目标识别模块由单个重链可变区(vhh)组成,分子量仅为12-14kd,有望克服传统单抗实体瘤穿透性低的缺陷。纳米抗体可与fc等功能结构域、其他纳米体、或多肽标签或毒素进行连接。由于其体积小,具有更高的扩散率,血管通透性、血脑等体内屏障的穿透力、以及肿瘤穿透力强等特点,比传统的单克隆抗体具有更均匀的组织分布。这些特性使它们特别适合于体内特定和有效的肿瘤靶向治疗。纳米抗体还具有免疫原性低、稳定性高、降解抗性高、原核生物表达生产成本低、产品表征容易等优势。不过,尽管众多的潜在优势,基于纳米抗体的肿瘤治疗药物开发迄今尚处于早期探索研究阶段。
3、近年来,抗体-药物偶联物(antibody-drug conjugate,adc)已成为肿瘤治疗的新风向。adc是利用单克隆抗体特异性识别肿瘤细胞表面特定抗原的特点,从而实现精准地将抗肿瘤药物(如小分子化疗药物等)递送到肿瘤靶细胞并释放,达到精准杀伤肿瘤的目的。但是由于adc分子量大,瘤内穿透力较弱等限制,导致在肿瘤内药物吸收分布效果有限且差异大,实体瘤应用不够理想。并且adc在体内循环系统的终末半衰期长,这可导致荷载毒素对正常组织或细胞产生不必要的毒性。而通过纳米抗体制备的纳米抗体-药物偶联物(nanobody-drug conjugate,ndc)不仅保留了传统adc的优点,还具有血管通透性高、血脑等屏障穿透性好、肿瘤穿透力强、到达靶细胞速度快,可以提高药物在肿瘤的累积,同时还可适度控制药物的血浆暴露量及半衰期,有助于进一步提高对实体瘤的治疗效果和整体治疗窗,有望成为最具潜力的一类全新的抗肿瘤药物。
4、综上所述,基于tf在肿瘤发展和复发耐药等机制中的重要作用,开发靶向tf-nb及tf-ndc药物能够为临床上单独或联合治疗tf异常表达的肿瘤患者提供新的治疗策略。
技术实现思路
1、本发明的目的在于提供一种靶向tf的纳米抗体及纳米抗体-药物偶联物、其制备方法和用途。
2、在本发明的第一方面,提供了一种靶向tf的纳米抗体,所述纳米抗体的vhh链的互补决定区cdr为选自下组的一种或多种:
3、(1)seq id no.1所示的cdr1,
4、seq id no.2所示的cdr2,和
5、seq id no.3所示的cdr3;
6、或者,
7、(2)seq id no.5所示的cdr1,
8、seq id no.6所示的cdr2,和
9、seq id no.7所示的cdr3;
10、或者,
11、(3)seq id no.9所示的cdr1,
12、seq id no.10所示的cdr2,和
13、seq id no.11所示的cdr3,
14、或者,
15、(4)seq id no.13所示的cdr1,
16、seq id no.14所示的cdr2,和
17、seq id no.15所示的cdr3,
18、或者,
19、(5)seq id no.17所示的cdr1,
20、seq id no.18所示的cdr2,和
21、seq id no.19所示的cdr3,
22、或者,
23、(6)seq id no.21所示的cdr1,
24、seq id no.22所示的cdr2,和
25、seq id no.23所示的cdr3,
26、或者,
27、(7)seq id no.25所示的cdr1,
28、seq id no.26所示的cdr2,和
29、seq id no.27所示的cdr3,
30、或者,
31、在另一优选例中,上述氨基酸序列中任意一种氨基酸序列还包括任选地经过添加、缺失、修饰和/或取代至少一个氨基酸的,并能够保留tf结合亲和力的衍生序列。
32、在另一优选例中,所述的纳米抗体vhh链的cdr区包含与上述中任一所述cdr区具有至少80%、优选地至少90%、更优选地至少95%、甚至更优选地至少99%的序列相似性的氨基酸序列。
33、在另一优选例中,所述的纳米抗体vhh链cdr区的氨基酸序列与上述中任一所述cdr区中任一相比包含一个或多个氨基酸取代,优选保守氨基酸取代。
34、在另一优选例中,所述vhh链包含选自下组的cdrl、cdr2和cdr3:
35、(1)seq id no.1、seq id no.2、seq id no.3所示的互补决定区cdr1、cdr2、cdr3(对应纳米抗体4-a02的cdr);或
36、(2)seq id no.5、seq id no.6、seq id no.7所示的互补决定区cdr1、cdr2、cdr3(对应纳米抗体f1-a01的cdr);或
37、(3)seq id no.9、seq id no.10、seq id no.11所示的互补决定区cdr1、cdr2、cdr3(对应纳米抗体4-c08的cdr);或
38、(4)seq id no.13、seq id no.14、seq id no.15所示的互补决定区cdr1、cdr2、cdr3(对应纳米抗体4-e04的cdr);或
39、(5)seq id no.17、seq id no.18、seq id no.19所示的互补决定区cdr1、cdr2、cdr3(对应纳米抗体4-c05的cdr);或
40、(6)seq id no.21、seq id no.22、seq id no.23所示的互补决定区cdr1、cdr2、cdr3(对应纳米抗体5-c12的cdr);或
41、(7)seq id no.25、seq id no.26、seq id no.27所示的互补决定区cdr1、cdr2、cdr3(对应纳米抗体5-h3的cdr)
42、在另一优选例中,所述的cdr1、cdr2和cdr3由vhh链的框架区fr1、fr2、fr3和fr4所隔开。
43、在另一优选例中,所述的纳米抗体包括人源化抗体、骆驼源抗体、嵌合抗体。
44、在另一优选例中,所述纳米抗体的vhh链还包括框架区(fr)。
45、在另一优选例中,所述的框架区fr为人源、鼠源、兔源或骆驼源。
46、在另一优选例中,所述的框架区fr包括人源的fr区、鼠源或骆驼源的fr区。
47、在另一优选例中,所述靶向tf的纳米抗体的vhh链具有选自下组的氨基酸序列:seq id no.4、seq id no.8、seq id no.12、seq id no.16、seq id no.20、seq id no.24、seq id no.28。
48、在另一优选例中,所述的纳米抗体序列包含与seq id no.4、seq id no.8、seq idno.12、seq id no.16、seq id no.20、seq id no.24、seq id no.28具有至少80%、优选地至少90%、更优选地至少95%、甚至更优选地至少99%的序列相似性的氨基酸序列。
49、在本发明的第二方面,提供了一种靶向tf的抗体,所述抗体包括一个或多个如本发明第一方面所述的靶向tf的纳米抗体的vhh链。
50、在另一优选例中,所述靶向tf的纳米抗体的vhh链具有选自下组的氨基酸序列:seq id no.4、seq id no.8、seq id no.12、seq id no.16、seq id no.20、seq id no.24、seq id no.28。
51、在另一优选例中,所述抗体为单体、二价抗体、和/或多价抗体。
52、在另一优选例中,所述抗体为动物源抗体、人源化抗体、嵌合抗体或嵌合抗原受体抗体(car)。
53、在另一优选例中,所述人源化抗体的cdr区包含1、2、或3个氨基酸的变化。
54、在另一优选例中,所述的动物为非人哺乳动物,较佳地为鼠、羊、兔、骆驼。
55、在另一优选例中,所述的抗体为双链抗体、或单链抗体。
56、在另一优选例中,所述的抗体为单克隆抗体。
57、在另一优选例中,所述的抗体是部分或全人源化的单克隆抗体。
58、在另一优选例中,所述添加、缺失、修饰和/或取代的氨基酸数量,不超过初始氨基酸序列总氨基酸数量的40%,较佳地为20%,更佳地为10%。
59、在另一优选例中,所述添加、缺失、修饰和/或取代的氨基酸数量为1-7个,较佳地为1-3个,更佳地为1个。
60、在另一优选例中,所述经过添加、缺失、修饰和/或取代的至少一个氨基酸序列为同源性为至少80%的氨基酸序列。
61、在另一优选例中,所述经过添加、缺失、修饰和/或取代至少一个氨基酸的衍生序列具有抑制细胞表面tf或重组tf蛋白的生物学功能。
62、在另一优选例中,所述的抗体为药物偶联物形式。
63、在另一优选例中,所述纳米抗体对人tf蛋白胞外区(tf-ecd)经fortebio表面等离子体共振(spr)测定的结合常数kd值为0.202~7.04nm。
64、在另一优选例中,所述抗体具有选自下组的一个或多个特性:
65、(a)特异结合肿瘤细胞,和/或肿瘤微环境中的免疫/基质细胞的tf;
66、(b)特异性抑制肿瘤tf相关的肿瘤细胞信号通路;
67、(c)改善tf过度激活所造成的细胞因子分泌的紊乱;
68、(d)抑制肿瘤细胞迁移或转移;
69、(e)抑制肿瘤生长,提高联合用药的抗肿瘤疗效;
70、(f)促进免疫细胞的增殖存活及功能,从而提高肿瘤免疫的效果;
71、(g)结合肿瘤细胞后被内吞至细胞内溶酶体;
72、(h)具有穿透血脑屏障、脑内高效分布的特性;
73、(i)针对脑部肿瘤具有良好的治疗效果;
74、(j)针对多种实体瘤具有良好的治疗效果。
75、在本发明的第三方面,提供了一种多特异性抗体,所述的多特异性抗体包含:本发明第一方面所述的靶向tf的纳米抗体或本发明第二方面所述的靶向tf的抗体。
76、在另一优选例中,多特异性抗体还包括靶向选自下组的靶点的第二抗原结合区:egfr、tgfβ、bcma、b7h6、gucy2c、dll3、cd38、cd123、cd19、cd20、cd22、b7-h3、gpc3、her2、pmsa、cd28、4-1bb、ox40、cd40、cd27、cd3、ctla4、pd1、pdl1、cd73、bcma、glp-1、trop2、tigit、lag-3、fgl1、tlr7,或其组合。
77、在另一优选例中,所述的第二抗原结合区为纳米抗体。
78、在另一优选例中,所述多特异性抗体包括一个或多个第二抗原结合区。
79、在另一优选例中,所述多特异性抗体还包含抗体的fc段。
80、在另一优选例中,所述抗原结合区为抗体或抗体片段,所述抗体片段包括:(i)fab片段;(ii)f(ab')2片段;(iii)fd片段;(iv)fv片段;(v)单链fv(scfv)分子;(vi)dab片段。
81、本发明的第四方面,提供了一种重组蛋白,所述的重组蛋白具有:
82、(i)靶向tf的纳米抗体,如本发明第一方面所述的靶向tf的纳米抗体、如本发明第二方面所述的抗tf抗体或如本发明第三方面所述的多特异性抗体;以及
83、(ii)任选的具有治疗功能的多肽分子或片段;和/或
84、(iii)任选的提升蛋白理化性质或成药性的功能域。
85、在另一优选例中,所述提升蛋白理化性质或成药性包括延长靶向tf的纳米抗体的半衰期。
86、在另一优选例中,所述重组蛋白还包括:(iv)任选的协助表达和/或纯化的标签序列。
87、在另一优选例中,所述的标签序列选自下组:6his标签、gggs序列、flag标签。
88、在另一优选例中,所述的重组蛋白为单体、二聚体、或多聚体。
89、在另一优选例中,所述具有治疗功能的多肽分子或片段包括但不限于:靶向egfr、tgfβ、bcma、b7h6、gucy2c、dll3、cd38、cd123、cd19、cd20、cd22、b7-h3、gpc3、her2、pmsa、cd28、4-1bb、ox40、cd40、cd27、cd3、ctla4、pd1、pdl1、cd73、bcma、glp-1、trop2、tigit、lag-3、fgl1、tlr7的多肽分子或片段。
90、在另一优选例中,所述具有治疗功能的多肽分子或片段包括但不限于:胰岛素、il-2、干扰素、降钙素、ghrh肽、肠肽类似物、白蛋白、抗体片段、细胞因子。
91、在另一优选例中,所述的重组蛋白(或多肽)包括融合蛋白。
92、在另一优选例中,所述的融合蛋白包括多特异性抗体、嵌合抗体。
93、在另一优选例中,所述提升蛋白理化性质或成药性的功能域包括fc段、抗白蛋白纳米抗体(hle)、白蛋白结合域(abd)。
94、在另一优选例中,所述的重组蛋白从n-c端或c-n端具有如下结构:
95、(a-b)m;
96、其中,a元件为靶向tf的纳米抗体;
97、b元件为fc段、人白蛋白结合域(abd)或抗白蛋白纳米抗体(hle);
98、“-”代表肽键或接头,
99、其中,m为正整数。
100、在另一优选例中,所述接头为刚性接头或柔性接头。
101、在另一优选例中,所述b元件还包括任选的提升蛋白理化性质或成药性的功能域,或任选的协助表达和/或纯化的标签序列。
102、在另一优选例中,m为1、2、3或4。
103、在另一优选例中,所述靶向tf的纳米抗体为如本发明第一方面所述的靶向tf的纳米抗体、如本发明第二方面所述的抗tf抗体或如本发明第三方面所述的多特异性抗体。
104、在另一优选例中,所述靶向tf的纳米抗体的vhh链具有选自下组的氨基酸序列:
105、seq id no.4、seq id no.8、seq id no.12、seq id no.16、seq id no.20、seq idno.24、seq id no.28。
106、在另一优选例中,所述fc段为人igg fc段,较佳地来自人igg1、或人igg2。
107、在另一优选例中,所述fc段选自fc1、fcwt或fclalapg;其中,
108、所述fc1的序列如seq id no.29的第115-346位所示。
109、所述fcwt的序列如seq id no.30的第115-346位所示。
110、所述fclalapg的序列如seq id no.31的第115-346位所示。
111、在另一优选例中,所述abd的氨基酸序列如seq id no.32的第130-198位所示。
112、在另一优选例中,所述重组蛋白具有选自下组的氨基酸序列:seq id no.29、seqid no.30、seq id no.31、seq id no.32。
113、本发明的第五方面,提供了一种car构建物,所述的car构建物的抗原结合区域为如本发明第一方面所述的纳米抗体的vhh链。
114、本发明的第六方面,提供了一种重组的免疫细胞,所述的免疫细胞表达外源的如本发明的第五方面所述的car构建物。
115、在另一优选例中,所述的免疫细胞选自下组:nk细胞、t细胞。
116、在另一优选例中,所述的免疫细胞来自人或非人哺乳动物(如鼠)。
117、本发明的第七方面,提供了一种免疫偶联物,所述的免疫偶联物含有:
118、(a)抗体部分,所述抗体部分为本发明第一方面所述的靶向tf的纳米抗体或本发明第二方面所述的靶向tf的抗体;和
119、(b)与所述纳米抗体部分偶联的偶联部分,所述偶联部分选自下组:可检测标记物、药物、毒素、细胞因子、酶、蛋白降解剂、寡核苷酸或其组合。
120、在另一优选例中,所述免疫偶联物为纳米抗体药物偶联物(ndc)。
121、在另一优选例中,所述的纳米抗体部分与所述的偶联部分通过化学键或接头进行偶联。
122、在另一优选例中,所述的偶联部分为化学标记和生物标记。
123、在另一优选例中,所述化学标记为同位素、免疫毒素和/或化学药物。
124、在另一优选例中,所述生物标记为生物素、亲和素或酶标记。
125、在另一优选例中,所述偶联部分为药物或毒素。
126、在另一优选例中,所述的药物为细胞毒性药物。
127、在另一优选例中,所述的细胞毒性药物选自下组:抗微管蛋白药物、dna小沟结合试剂、dna复制抑制剂、烷化试剂、抗生素、叶酸拮抗物、抗代谢药物、化疗增敏剂、拓扑异构酶抑制剂、长春花生物碱、或其组合。
128、特别有用的细胞毒性药物类的例子包括,例如,dna小沟结合试剂、dna烷基化试剂、和微管蛋白抑制剂、典型的细胞毒性药物包括、例如奥瑞他汀(auristatins)、喜树碱(camptothecins)、多卡霉素/倍癌霉素(duocarmycins)、依托泊甙(etoposides)、美登木素(maytansines)和美登素类化合物(maytansinoids)(例如dm1和dm4)、紫杉烷(taxanes)、苯二氮卓类(benzodiazepines)或者含有苯二氮卓的药物(benzodiazepine containingdrugs)(例如吡咯并[1,4]苯二氮卓类(pbds),吲哚啉苯并二氮卓类(indolinobenzodiazepines)和噁唑烷并苯并二氮卓类(oxazolidinobenzodiazepines))、长春花生物碱(vinca alkaloids)、或其组合。
129、在另一优选例中,所述的毒素选自下组:
130、耳他汀类(例如,耳他汀e、耳他汀f、mmae和mmaf)、金霉素、类美坦西醇、篦麻毒素、篦麻毒素a-链、考布他汀、多卡米星、多拉司他汀、阿霉素、柔红霉素、紫杉醇、顺铂、cc1065、溴化乙锭、丝裂霉素、依托泊甙、替诺泊甙(tenoposide)、长春新碱、长春碱、秋水仙素、二羟基炭疽菌素二酮、放线菌素、白喉毒素、假单胞菌外毒素(pe)a、pe40、相思豆毒素、相思豆毒素a链、蒴莲根毒素a链、α-八叠球菌、白树毒素、迈托毒素(mitogellin)、局限曲菌素(retstrictocin)、酚霉素、依诺霉素、麻疯树毒蛋白(curicin)、巴豆毒素、卡奇霉素、肥皂草(sapaonaria officinalis)抑制剂、糖皮质激素、或其组合。
131、在另一优选例中,所述偶联部分为可检测标记物。
132、在另一优选例中,所述可检测标记物包括放射性核素,所述的放射性核素包括:
133、(i)诊断用同位素,所述的诊断用同位素选自下组:tc-99m、ga-68、f-18、i-123、i-125、i-131、in-111、ga-67、cu-64、zr-89、c-11、lu-177、re-188、或其组合;和/或
134、(ii)治疗用同位素,所述的治疗用同位素选自下组:lu-177、y-90、ac-225、as-211、bi-212、bi-213、cs-137、cr-51、co-60、dy-165、er-169、fm-255、au-198、ho-166、i-125、i-131、ir-192、fe-59、pb-212、mo-99、pd-103、p-32、k-42、re-186、re-188、sm-153、ra223、ru-106、na24、sr89、tb-149、th-227、xe-133 yb-169、yb-177、或其组合。
135、在另一优选例中,所述蛋白降解剂为肿瘤相关蛋白的降解剂,所述肿瘤相关蛋白选自下组:egfr、nf-κb、ripk2、bcr-abl、her2、c-met、tbk1、cdk、alk、akt、ck2、erk1/2、flt3、pi3k、btk、trk、fak、brd、ar、er、metap-2、bcl-xl、sirt2、hdac6、pirin、smad3、arnt、pcaf/gcn5、tau、ezh2、irak4、stat3frs2、ras(例如kras、hras和nras)。
136、在另一优选例中,所述kras包括kras-g12c、kras-g12d、kras-g12v等。
137、在另一优选例中,所述蛋白降解剂包括protac(蛋白降解靶向嵌合体)。
138、在另一优选例中,所述protac靶向egfr、kras(包括kras-g12c、kras-g12d、kras-g12v等)。
139、在另一优选例中,所述寡核苷酸包括反义寡核苷酸(aso)、小干扰rna(sirna)、微小rna(mirna)、小激活rna(sarna)、信使rna(mrna)或rna适配(aptamer)。
140、在另一优选例中,所述偶联物选自:荧光或发光标记物、放射性标记物、mri(磁共振成像)或ct(电子计算机x射线断层扫描技术)造影剂、或能够产生可检测产物的酶、放射性核素、生物毒素、细胞因子(如il-2等)、抗体、抗体fc片段、抗体scfv片段、金纳米颗粒/纳米棒、病毒颗粒、脂质体、纳米磁粒、前药激活酶(例如,dt-心肌黄酶(dtd)或联苯基水解酶-样蛋白质(bphl))、化疗剂(例如,顺铂)或任何形式的纳米颗粒等。
141、在另一优选例中,所述免疫偶联物含有:多价(如二价)的如本发明的第一方面所述的靶向tf的纳米抗体或本发明的第二方面所述的靶向tf的抗体。
142、在另一优选例中,所述多价是指,在所述免疫偶联物的氨基酸序列中包含多个重复的如本发明的第一方面所述的靶向tf的纳米抗体或本发明的第二方面所述的靶向tf的抗体。
143、在另一优选例中,所述的检测为体内检测或体外检测。
144、在另一优选例中,所述免疫偶联物用于诊断和/或治疗表达tf蛋白的肿瘤。
145、在另一优选例中,所述抗体药物偶联物adc如下分子式所示:
146、
147、其中:
148、nab是靶向tf的纳米抗体或如本发明第四方面所述的重组蛋白,
149、lu是接头2(又称连接子);
150、d是药物;
151、而且下标p是选自1-8的值。
152、在另一优选例中,所述nab为如本发明第四方面所述的重组蛋白。
153、在另一优选例中,所述抗体药物偶联物adc为单体、二聚体或多聚体。
154、在另一优选例中,所述的重组蛋白从n-c端或c-n端具有如下所示的结构:
155、(a-l1-b)m;
156、其中,a元件为靶向tf的纳米抗体;
157、b元件为fc段、人白蛋白结合域(abd)或抗白蛋白纳米抗体(hle);
158、“l1”代表无或接头1,
159、其中,m为正整数。
160、在另一优选例中,m为1、2、3或4。
161、在另一优选例中,所述药物定点连接于靶向tf的纳米抗体的末端氨基或侧链氨基或巯基。
162、在另一优选例中,所述药物定点和/或随机地连接于所述靶向tf的纳米抗体。
163、在另一优选例中,所述药物定点连接于所述a元件、b元件或l1。
164、在另一优选例中,所述药物定点连接于b元件和/或l1。
165、在另一优选例中,所述药物定点连接于b元件的末端氨基或巯基;和/或连接于l1的侧链氨基或巯基。
166、在另一优选例中,b元件为fc段,所述药物定点连接于fc段的铰链区(hinge)和/或fc段的c端。
167、在另一优选例中,b元件为人白蛋白结合域(abd),所述药物定点连接于abd的c端。
168、在另一优选例中,b元件为hle,所述药物定点连接于hle的c端。
169、在另一优选例中,所述抗体药物偶联物adc具有选自图24中的结构。
170、在另一优选例中,lu选自马来酰亚胺基己酰基(mc)、马来酰亚胺(mal)、琥珀酰亚胺基4-(n-马来酰亚胺甲基)环己烷-1-甲酸酯)(smcc)接头与抗体部分连接,并包含缬氨酸-瓜氨酸(vc)、缬氨酸-丙氨酸(va)、甘氨酸-甘氨酸-苯丙氨酸-甘氨酸(ggfg)、丙氨酸-丙氨酸-丙氨酸(aaa)、对氨基苄氧基羰基(pab)、聚乙二醇(peg)的一种或多种的连接子。
171、在另一优选例中,其中所述抗体通过与选自下组的部分反应共价结合至所述接头:马来酰亚胺基己酰基(mc)、马来酰亚胺(mal)、琥珀酰亚胺基4-(n-马来酰亚胺甲基)环己烷-1-甲酸酯)(smcc)。
172、在另一优选例中,其中d选自下组具有抗肿瘤活性的化合物:
173、(i)微管蛋白抑制剂,如美登素衍生物(dm1、dm4),单甲基奥瑞他汀e(mmae)、单甲基奥瑞他汀f(mmaf);
174、(ii)作用于dna毒素,如倍癌霉素(duocarmycin)、吡咯并苯二氮卓(pbd);
175、(iii)拓扑异构酶抑制剂,喜树碱、sn38、依喜替康、dxd。
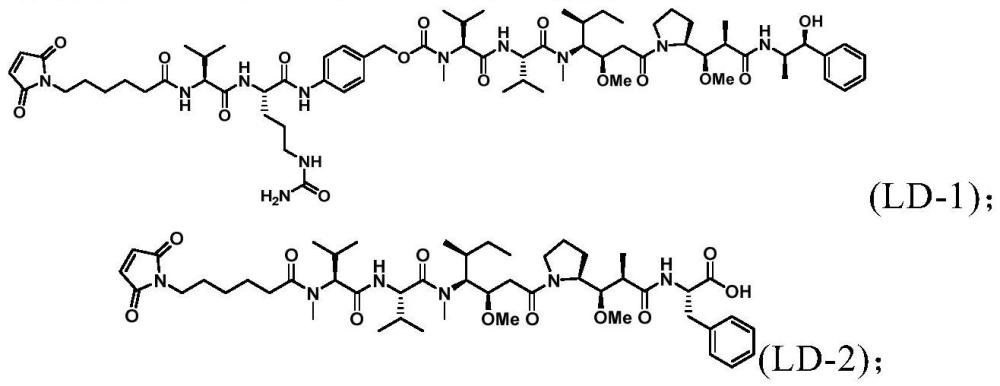
176、在另一优选例中,其中所述lu-d化合物选自下组:
177、
178、
179、本发明的第八方面,提供了一种药物组合物,所述的药物组合物包含:
180、(i)如本发明的第一方面所述的靶向tf的纳米抗体、如本发明的第二方面所述的靶向tf的抗体、如本发明的第三方面的多特异性抗体、如本发明的第四方面所述的重组蛋白、如本发明的第六方面所述的重组的免疫细胞或如本发明的第七方面所述的免疫偶联物;
181、(ii)药学上可接受的载体。
182、在另一优选例中,所述的药物组合物包括单方药物、复方药物、或协同药物。
183、在另一优选例中,所述的药物组合物还包含其他生物活性物质,如治疗肿瘤的药物。
184、在另一优选例中,所述的药物组合物的施用方式选自下组:皮下注射、皮内注射、肌肉注射、静脉注射、腹腔注射、微针注射、口服、或口鼻腔喷入和雾化吸入。
185、在另一优选例中,所述的药物组合物的剂型选自下组:液态、固体、或凝胶态。
186、在另一优选例中,所述的药物组合物为液态制剂。
187、在另一优选例中,所述的药物组合物为注射剂。
188、本发明的第九方面,提供了一种活性成分的用途,所述的活性成分选自下组:如本发明的第一方面所述的靶向tf的纳米抗体、如本发明的第二方面所述的靶向tf的抗体、如本发明的第三方面的多特异性抗体、如本发明的第四方面所述的重组蛋白、如本发明的第六方面所述的重组的免疫细胞、如本发明的第七方面所述的免疫偶联物、或其组合,所述活性成分用于(a)制备检测试剂、检测板或试剂盒;和/或(b)制备预防和/或治疗tf相关疾病的药物。
189、在另一优选例中,所述检测试剂、检测板或试剂盒用于:
190、(1)检测样品中的tf蛋白;和/或
191、(2)检测肿瘤细胞中内源性的tf蛋白;和/或
192、(3)检测表达tf蛋白的肿瘤细胞。
193、在另一优选例中,所述的检测类型,包括但不限于用于流式检测、细胞免疫荧光检测、酶联免疫吸附检测、免疫印迹检测等。
194、在另一优选例中,所述的检测试剂、检测板或试剂盒用于诊断tf相关疾病。
195、在另一优选例中,所述的药物用于治疗或预防tf高表达的肿瘤、肿瘤迁移、或肿瘤耐药。
196、在另一优选例中,所述的肿瘤耐药包括:肿瘤免疫治疗药物的耐药、肿瘤靶向治疗药物的耐药、常规肿瘤化疗的耐药,放射治疗的不敏感。
197、在另一优选例中,所述的药物用于选自下组的用途:
198、(a)特异结合肿瘤细胞,和/或肿瘤微环境中的免疫/基质细胞的tf;
199、(b)特异性抑制肿瘤tf相关的肿瘤细胞信号通路;
200、(c)改善tf过度激活所造成的细胞因子分泌的紊乱;
201、(d)抑制肿瘤细胞迁移或转移;
202、(e)抑制肿瘤生长,提高联合用药的抗肿瘤疗效;
203、(f)促进免疫细胞的增殖存活及功能,从而提高肿瘤免疫的效果;
204、(g)结合肿瘤细胞后被内吞至细胞内溶酶体;
205、(h)具有穿透血脑屏障、脑内高效分布的特性;
206、(i)针对脑部肿瘤具有良好的治疗效果;
207、(j)针对多种实体瘤具有良好的治疗效果。
208、在另一优选例中,所述tf相关疾病选自下组:癌症、血栓、自身免疫疾病、代谢相关疾病、感染疾病、或其组合。
209、在另一优选例中,所述tf相关的疾病包括:肿瘤的发生、生长和/或转移。
210、在另一优选例中,所述的癌症包括实体瘤、血液癌。
211、在另一优选例中,所述的癌症为tf高表达的肿瘤。
212、在另一优选例中,所述的tf高表达的肿瘤选自下组:乳腺癌、肺癌、胰腺癌、卵巢癌、宫颈癌、直肠癌、脑胶质瘤、黑色素瘤、白血病、淋巴瘤、或其组合。
213、在另一优选例中,所述的癌症为耐药性肿瘤。
214、在另一优选例中,所述的tf高表达的肿瘤指肿瘤组织中tf转录本和/或蛋白的水平l1与正常组织中转录本和/或蛋白的水平l0之比,l1/l0≥2,较佳地≥3。
215、本发明的第十方面,提供了一种多核苷酸,其特征在于,所述的多核苷酸编码选自下组的多肽:
216、(1)本发明的第一方面所述的靶向tf的纳米抗体、本发明的第二方面所述的靶向tf的抗体、或如本发明的第三方面的多特异性抗体;
217、(2)如本发明的第四方面所述的重组蛋白;或
218、(3)如本发明的第五方面所述的car构建物。
219、在另一优选例中,所述多核苷酸包括rna、dna或cdna。
220、本发明的第十一方面,提供了一种载体,其特征在于,所述的载体含有如本发明的第十方面所述的多核苷酸。
221、在另一优选例中,所述的载体包括:细菌质粒、噬菌体、酵母质粒、植物细胞病毒、哺乳动物细胞病毒如腺病毒、逆转录病毒、或其他载体。
222、本发明的第十二方面,提供了一种遗传工程化的宿主细胞,其特征在于,所述的宿主细胞含有本发明的第十一方面所述的载体或基因组中整合有本发明的第十方面所述的多核苷酸。
223、本发明的第十三方面,提供了一种体外检测(包括诊断性或非诊断性)样品中tf的方法,其特征在于,所述方法包括步骤:
224、(1)在体外,将所述样品与本发明的第一方面所述的靶向tf的纳米抗体、本发明的第二方面所述的靶向tf的抗体或如本发明的第七方面所述的免疫偶联物接触;
225、(2)检测是否形成抗原-抗体复合物,其中形成复合物就表示样品中存在tf。
226、在另一优选例中,所述的检测包括诊断性的或非诊断性的。
227、本发明的第十四方面,提供了一种检测板,所述的检测板包括:基片(支撑板)和测试条,所述的测试条含有本发明第一方面所述的靶向tf的纳米抗体或本发明第二方面所述的靶向tf的抗体或本发明第七方面所述的免疫偶联物。
228、本发明的第十五方面,提供了一种试剂盒,所述试剂盒中包括:
229、(1)第一容器,所述第一容器中含有本发明第一方面所述的靶向tf的纳米抗体或本发明第二方面所述的靶向tf的抗体;和/或
230、(2)第二容器,所述第二容器中含有抗本发明第一方面所述的靶向tf的纳米抗体或本发明第二方面所述的靶向tf的抗体的二抗;
231、或者,所述试剂盒含有本发明第十四方面所述的检测板。
232、本发明的第十六方面,提供了一种重组多肽的制备方法,其特征在于,所述方法包括:
233、(a)在适合表达的条件下,培养本发明的第十二方面所述的宿主细胞;
234、(b)从培养物中分离出重组多肽,所述的重组多肽是如本发明的第一方面所述的靶向tf的纳米抗体、如本发明的第二方面所述的靶向tf的抗体、如本发明的第三方面的多特异性抗体、如本发明的第四方面所述的重组蛋白。
235、本发明的第十七方面,提供了一种治疗tf相关疾病的方法,其特征在于,所述方法包括:给需要的对象施用如本发明的第一方面所述的靶向tf的纳米抗体、如本发明的第二方面所述的靶向tf的抗体、如本发明的第三方面的多特异性抗体、如本发明的第四方面所述的重组蛋白、如本发明的第六方面所述的重组的免疫细胞、如本发明的第七方面所述的免疫偶联物、如本发明的第八方面所述的药物组合物、或其组合。
236、在另一优选例中,所述的方法还包括:给需要的对象施用其他药物或治疗方法进行联合治疗。
237、在另一优选例中,所述的其他药物或治疗方法包括:抗肿瘤免疫治疗药物、肿瘤靶向药物、肿瘤化疗药物、肿瘤放射治疗。
238、在另一优选例中,所述的抗肿瘤免疫治疗药物包括pd-1、pd-l1单抗。
239、在本发明的第十八方面,提供了一种制备嵌合抗体的方法,包括步骤:
240、将本发明第一方面所述的靶向tf的纳米抗体的羊驼来源的vhh序列的核苷酸序列克隆入含有人抗体恒定区的核苷酸序列的表达载体后,通过转染动物细胞表达人-羊驼嵌合抗体。
241、在本发明的第十九方面,提供了一种制备人源化抗体的方法,包括步骤:
242、将本发明第一方面所述的靶向tf的纳米抗体的vhh链的cdr区的核苷酸序列植入含人源抗体fr区的核苷酸序列模板,再将其克隆入含有人抗体恒定区的表达载体后,通过转染动物细胞表达人源化抗体。
243、在本发明的第二十方面,提供了一种抑制肿瘤细胞生长和迁移的方法,包括步骤:给需要的对象施用本发明的第一方面所述的靶向tf的纳米抗体、本发明的第二方面所述的靶向tf的抗体或本发明所述的纳米抗体-药物偶联物、或所述纳米抗体的car-t细胞、或其组合。
244、在本发明的第二十一方面,提供了一种抑制肿瘤在模型动物体内生长的方法,包括步骤:给需要的对象施用本发明的第一方面所述的靶向tf的纳米抗体、本发明的第二方面所述的靶向tf的抗体、本发明所述的纳米抗体-药物偶联物、或所述纳米抗体的car-t细胞。
245、在另一优选例中,所述药物可以实施单独给药,或组合用药包括肿瘤免疫疗法、肿瘤靶向药物、细胞毒药物、放射治疗。
246、在本发明的第二十二方面,提供了一种本发明的第七方面所述的纳米抗体-药物偶联物的制备方法,包括步骤:
247、(1)用抗体与还原试剂在缓冲液中反应,得到经还原后的抗体;
248、(2)用式dl连接子-药物缀合物与步骤(1)中得到的经还原后的抗体在缓冲液与有机溶剂混合液中进行交联(偶联),得到具有不同dar值的抗体-药物偶联物1a、1b、1c或1d。
249、在另一优选例中,所述制备方法的交联反应如图23所示。
250、在另一优选例中,所述步骤(1)中所述抗体经还原试剂还原,从而使抗体链间二硫键被还原,产生巯基基团。
251、在另一优选例中,所述步骤(1)中还原试剂为三(2-羧乙基)膦盐酸盐(tcep)、beta-巯基乙醇、beta-巯基乙胺盐酸盐、或二硫苏糖醇(dtt)。
252、在另一优选例中,所述的缓冲液选自下组:磷酸二氢钾-氢氧化钠(kh2po4-naoh)/氯化钠(nacl)/二乙基三胺五乙酸(dtpa)缓冲液、磷酸氢二钠-柠檬酸/氯化钠(nacl)/二乙基三胺五乙酸(dtpa)、硼酸-硼砂/氯化钠(nacl)/二乙基三胺五乙酸(dtpa)、组氨酸-氢氧化钠/氯化钠(nacl)/二乙基三胺五乙酸(dtpa),和pbs/二乙基三胺五乙酸(dtpa)。
253、在另一优选例中,所述的步骤(2)中,有机溶剂在反应液中的体积占比不超过15%。
254、在另一优选例中,所述的步骤(2)中的有机溶剂选自下组:乙腈(acn)、二甲基甲酰胺(dmf)、二甲基乙酰胺(dma)、二甲基亚砜(dmso)。
255、再加入连接子药物(预先10mg/ml溶在乙腈(acn)、二甲亚砜(dmso)、二甲基甲酰胺(dmf)或二乙基乙酰胺(dma)中),并保证反应液中有机溶剂的体积占比不超过15%,偶联反应于0-37℃搅动2-4小时。若采用tcep还原,也可不需除去剩余tcep,直接加入取代马来酰亚胺类化合物进行偶联。
256、采用脱盐柱将偶联反应混合物用琥珀酸钠/nacl缓冲液或组氨酸-醋酸/蔗糖凝胶过滤纯化,根据uv280紫外吸收值收集出峰样品。或超滤数遍。然后过滤除菌,所得产物低温保存。
257、所得抗体药物偶联物的药物抗体偶联比(dar)较为均一。对于dar有一定差别的ndc,如需要获得均一性更好的样品,可进一步利用但不限于以下方法进行分离纯化:疏水作用层析方法(hic)、分子排阻色谱法(sec)、离子交换层析(iec)。
258、应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
本文地址:https://www.jishuxx.com/zhuanli/20241021/317989.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表